L’immunoterapia moderna ha portato ad una rivoluzione nella gestione di molti tumori in precedenza privi di opzioni terapeutiche. L’introduzione dei cosiddetti Inibitori dei Checkpoint Immunitari (ICI) ha migliorato significativamente la sopravvivenza in diverse tipologie di cancro, tra cui il tumore della mammella e del polmone, il carcinoma a cellule renali ed il melanoma metastatico. Il loro profilo di sicurezza è generalmente considerato superiore rispetto alla chemioterapia citotossica e la qualità di risposta antitumorale è generalmente più prolungata e duratura (1). Tuttavia, parallelamente al crescente utilizzo, è stato segnalato un numero sempre più elevato di eventi collaterali, noti come Immune-related Adverse Events (irAE), che colpiscono numerosi organi, incluso il fegato.
Scudo e spada della terapia oncologica
L’attività antineoplastica degli ICI deriva dal loro effetto sui checkpoint immunitari, che normalmente servono a ridurre la risposta immunitaria e proteggere contro risposte autoimmuni. Normalmente, l’interazione tra la proteina B7 sulle cellule presentanti l’antigene (Antigen Presenting Cells, APC) e CD28 sulle cellule T (T cell) porta all’attivazione di queste ultime (Figura 1).
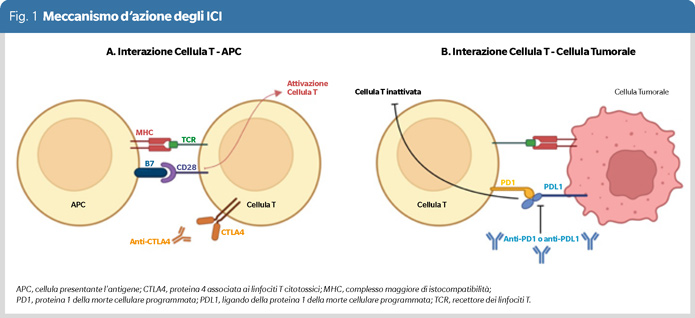
Il Cytotoxic T-lymphocyte Antigen 4 (noto come CTLA-4) presente sulle cellule T citotossiche, ha una forte affinità per B7, riduce la risposta delle cellule T dopo la stimolazione antigenica, competendo con CD28 per il legame a B7. Gli anticorpi monoclonali contro CTLA-4, come ipilimumab, bloccano la segnalazione inibitoria sui linfociti T citotossici, portando ad una attivazione del sistema immunitario, migliorando quindi la sua capacità di riconoscere e distruggere le cellule tumorali.
Quando le cellule T vengono attivate, aumentano l’espressione del recettore Programmed Cell Death-1 (comunemente noto come PD-1). Quando PD-1 sulle cellule T interagisce con Programmed Death-Ligand 1 (PD-L1) sulla cellula tumorale, le cellule T vengono inattivate. Gli anticorpi anti-PD-1, come pembrolizumab e nivolumab, e gli anticorpi anti- PD-L1, come atezolizumab e durvalumab, bloccano l’interazione tra PD-1 e i suoi ligandi, impedendo così l’inattivazione delle cellule T.
Sebbene questi anticorpi monoclonali contro CTLA-4 e PD-1/PD-L1 potenzino la risposta immunitaria specifica delle cellule T, possono anche causare vari effetti collaterali sistemici a causa di una risposta immunitaria non controllata. I meccanismi specifici che sono stati ipotizzati per spiegare la tossicità da ICI sono diversi: tossicità immunitaria diretta (PD-1, PDL-1 e CTLA-4 sono presenti anche nei tessuti sani), formazione di cellule B auto-reattive, reattività crociata tra antigeni tumorali e tessuti normali, ed infine deplezione di cellule T-regolatorie (2).
irAE: timing e presentazione clinica
La maggior parte degli irAE si manifesta entro i primi 60 giorni dall’inizio del trattamento, sebbene essi possano insorgere anche molti mesi dopo l’avvio o la conclusione dello stesso. Le tossicità più diffuse sono quelle coinvolgenti il tratto gastro-enterico (diarrea), la cute (rash cutaneo bolloso severo, dermatite infiammatoria, sindrome mani-piedi), il fegato (epatite), il sistema endocrino (ipo-ipertiroidismo, ipofisite) ed il polmone (polmonite) (3-6).
Ad oggi, i pazienti trattati con anti-PD1 o anti-PDL1 presentano un’incidenza minore di irAE rispetto a quelli trattati con anti-CTLA4 e soprattutto di coloro i quali ricevono terapie di combinazione (i.e. ICI + chemioterapia citotossica, combinazione di anti-PD1/PDL1 e anti-CTLA4). Rimanendo nell’ambito di competenza epatologica, l’incidenza dell’epatotossicità immunomediata in pazienti trattati con anti-CTLA4 si aggira attorno al 3-9% (7), con anti-PD1 all’1-3% (8), salendo al 18% in caso di terapie di combinazione anti-CTLA4 e anti-PD1 (9,10).
Epatite da ICI: quando sospettarla
 Poiché non esistono biomarcatori specifici per distinguere una tossicità epatica indotta da ICI, è bene inizialmente escludere tutte le cause classiche di epatite, tenendo anche conto della correlazione temporale tra l’esposizione agli ICI e il rialzo degli enzimi epatici. Da un punto di vista sintomatologico, alcuni pazienti possono manifestare dolore in ipocondrio destro, febbre o astenia, urine ipercromiche, sanguinamento, mentre altri possono essere completamente asintomatici. Esiste una griglia di valutazione della severità dell’epatotossicità da ICI in base a valori biochimici e sintomi, riportata nella tabella 1.
Poiché non esistono biomarcatori specifici per distinguere una tossicità epatica indotta da ICI, è bene inizialmente escludere tutte le cause classiche di epatite, tenendo anche conto della correlazione temporale tra l’esposizione agli ICI e il rialzo degli enzimi epatici. Da un punto di vista sintomatologico, alcuni pazienti possono manifestare dolore in ipocondrio destro, febbre o astenia, urine ipercromiche, sanguinamento, mentre altri possono essere completamente asintomatici. Esiste una griglia di valutazione della severità dell’epatotossicità da ICI in base a valori biochimici e sintomi, riportata nella tabella 1.
Da un punto di vista epidemiologico, in una recente analisi retrospettiva monocentrica (11), il 23.1% dei trattati con ICI ha sviluppato alterazioni degli esami di funzionalità epatica di grado 3, con danno epatico colestatico (60.3%), danno epatico epatocellulare (29.4%) e misto epatocellulare-colestatico (10.3%).
La recente approvazione di farmaci immunoterapici per la cura dell’epatocarcinoma pone nuove sfide gestionali, considerato che tale tumore insorge generalmente in pazienti affetti da cirrosi epatica, che possono manifestare alterazioni degli indici epatici per molteplici ragioni oltre al danno da farmaco.
Epatite da ICI vs epatite autoimmune
La presentazione clinica dell’epatotossicità da ICI potrebbe essere confusa con quella dell’epatite autoimmune (AIH).
È però bene notare che generalmente rispetto alla tossicità epatica da ICI:
- i pazienti AIH sono più giovani, di sesso femminile e hanno disturbi autoimmuni preesistenti
- i pazienti AIH hanno anticorpi antinucleo (ANA), anti-muscolo liscio (ASMA), anti-LKM 1 G positivi (ANA e ASMA possono essere positivi anche nel 50% dei pazienti con epatite da ICI, anche se in questi anti-LKM 1 sono negativi ed IgG normali) e valori elevati di immunoglobuline
- i pazienti AIH si presentano più spesso con epatopatia cronica sottostante e conta piastrinica inferiore se l’epatopatia cronica misconosciuta è già avanzata
- a differenza della tossicità epatica indotta dagli ICI, la AIH tende a recidivare durante la riduzione graduale della terapia steroidea, rendendo necessaria l’introduzione di un secondo farmaco immunosoppressivo.
 La biopsia epatica, sebbene raccomandata in pazienti con epatite di grado 3-4 (opzionale per pazienti con epatite di grado 2 [12]), non sempre permette di distinguere chiaramente tra AIH e tossicità epatica ICI indotta, presentando queste un danno istologico simile dovuto all’infiltrazione tissutale di cellule T CD8+.
La biopsia epatica, sebbene raccomandata in pazienti con epatite di grado 3-4 (opzionale per pazienti con epatite di grado 2 [12]), non sempre permette di distinguere chiaramente tra AIH e tossicità epatica ICI indotta, presentando queste un danno istologico simile dovuto all’infiltrazione tissutale di cellule T CD8+.
Il danno istologico da ICI può assomigliare a quello dell’AIH in termini di necrosi focale o confluente ed ampia infiltrazione linfocitaria di cellule T attivate (5, 13). Tuttavia, nella tossicità da ICI, la necrosi zonale centrolobulare (presente, comunque, solo nelle forme di AIH severe) e la plasmacitosi sono rare, così come il numero di linfociti CD20+ o CD4+ significativamente inferiore. Nel 2016, Champiat e coll. (14) hanno definito chiaramente gli aspetti chiave per gestire gli irAE durante il trattamento con ICI, che includono: attento monitoraggio dei pazienti, scelta del tipo di assistenza (ambulatoriale o ospedaliera), uso di trattamenti sintomatici, sospensione temporanea o definitiva dell’immunoterapia e, se necessario, somministrazione di steroidi o altri immunosoppressori (Tabella 2).
Considerando la scarsità di sintomi correlati al danno epatico, l’ASCO (American Society of Clinical Oncology) raccomanda di monitorare AST, ALT e bilirubina prima di ogni infusione e/o settimanalmente se si rileva un incremento di lieve entità nei test di funzionalità epatica (15).
Il rechallenge con ICI: una nuova sfida
Le linee guida internazionali raccomandano la sospensione permanente dell’immunoterapia in caso di epatite immunorelata di grado 3 o grado 4. Tuttavia, alcuni pazienti potrebbero trarre beneficio dalla continuazione della stessa: è bene sottolineare che gli eventi avversi immunorelati sono spesso associati ad una prognosi migliore della malattia oncologica sottostante.
Secondo le linee guida dell’European Society for Medical Oncology (ESMO), è possibile reintrodurre ICI dopo un’epatite immunorelata: l’utilizzo è lasciato alla discrezione del medico per il grado 3 mentre è vietato per il grado 4. Vari esempi di rechallenge sono stati riportati in letteratura (16-18), con tassi di ricorrenza molto variabili (dallo 0 al 60%), in base al tipo di molecola usata. Si può dunque concludere che la reintroduzione degli ICI in un paziente con storia di epatite immunorelata è possibile, anche nel caso di AIH ben controllata con singola o duplice terapia (19). Tuttavia, il rapporto rischio-beneficio deve essere attentamente considerato, poiché i fattori di rischio per la ricorrenza di epatite sono al momento poco chiari. È necessario valutare la severità di presentazione, la presenza di epatopatia cronica (sia da AIH cronica che da comorbidità come la malattia epatica associata a disfunzione metabolica (MASLD - Metabolic dysfunction-associated steatotic liver disease) o la malattia epatica alcolica (ALD - Alcoholic Liver Disease), le condizioni generali del paziente, la volontà del paziente, la prognosi oncologica e la probabilità di risposta all’immunoterapia.
Aspetti principali
- I farmaci ICI possono causare eventi avversi immunorelati in vari organi, incluso il fegato, più comunemente entro i primi 60 giorni di terapia
- L’epatotossicità è meno comune con anti-PD1/PDL1 rispetto ad anti-CTLA4, ed è più frequente con terapie combinate. In assenza di biomarcatori specifici, è necessario escludere altre cause di danno epatico acuto
- La valutazione del grado di epatotossicità si basa su severità della alterazione degli indici biochimici epatici e presenza e gravità dei sintomi correlati
- La gestione terapeutica include il monitoraggio laboratoristico e clinico, la sospensione temporanea o definitiva dell’ICI, e la somministrazione di steroidi o altri immunosoppressori in base alla severità ed al contesto clinico
- La reintroduzione degli ICI può essere intrapresa in base al rapporto rischio-beneficio che tenga in considerazione lo stato generale del paziente, le sue preferenze, la prognosi della malattia oncologica, e la presenza di una epatopatia cronica con rischio di complicanze epatiche in caso di riaccensione epatitica
- Borghaei H, Paz-Ares L, Horn L, et al. Nivolumab versus Docetaxel in Advanced Nonsquamous Non-Small-Cell Lung Cancer. N Engl J Med. 2015;373(17):1627-39.
- De Martin E, Michot JM, Rosmorduc O, et al. Liver toxicity as a limiting factor to the increasing use of immune checkpoint inhibitors. JHEP Rep. 2020;2(6):100170.
- Weber JS, Hodi FS, Wolchok JD, et al. Safety Profile of Nivolumab Monotherapy: A Pooled Analysis of Patients With Advanced Melanoma. J Clin Oncol. 2017;35(7):785-792.
- Abdel-Wahab N, Shah M, Suarez-Almazor ME. Adverse Events Associated with Immune Checkpoint Blockade in Patients with Cancer: A Systematic Review of Case Reports. PLoS One. 2016;11(7):e0160221.
- Zen Y, Yeh MM. Hepatotoxicity of immune checkpoint inhibitors: a histology study of seven cases in comparison with autoimmune hepatitis and idiosyncratic drug-induced liver injury. Mod Pathol. 2018;31(6):965-973.
- Schneider BJ, Naidoo J, Santomasso BD, et al. Management of Immune-Related Adverse Events in Patients Treated With Immune Checkpoint Inhibitor Therapy: ASCO Guideline Update. J Clin Oncol. 2021;39(36):4073-4126.
- Reddy HG, Schneider BJ, Tai AW. Immune Checkpoint Inhibitor-Associated Colitis and Hepatitis. Clin Transl Gastroenterol. 2018;9(9):180.
- Robert C, Ribas A, Wolchok JD, et al. Anti-programmed-death-receptor-1 treatment with pembrolizumab in ipilimumab-refractory advanced melanoma: a randomised dose-comparison cohort of a phase 1 trial. Lancet. 2014;384(9948):1109-17.
- Michot JM, Bigenwald C, Champiat S, et al. Immune-related adverse events with immune checkpoint blockade: a comprehensive review. Eur J Cancer. 2016;54:139-148.
- Lombardi A, Mondelli MU. Review article: immune checkpoint inhibitors and the liver, from therapeutic efficacy to side effects. Aliment Pharmacol Ther. 2019;50(8):872-884.
- Parlati L, Vallet-Pichard A, Batista R, et al. Incidence of grade 3-4 liver injury under immune checkpoints inhibitors: A retrospective study. J Hepatol. 2018;69(6):1396-1397.
- Puzanov I, Diab A, Abdallah K, et al. Managing toxicities associated with immune checkpoint inhibitors: consensus recommendations from the Society for Immunotherapy of Cancer (SITC) Toxicity Management Working Group. J Immunother Cancer. 2017;5(1):95.
- Johncilla M, Misdraji J, Pratt DS, et al. Ipilimumab-associated Hepatitis: Clinicopathologic Characterization in a Series of 11 Cases. Am J Surg Pathol. 2015;39(8):1075-84.
- Champiat S, Lambotte O, Barreau E, et al. Management of immune checkpoint blockade dysimmune toxicities: a collaborative position paper. Ann Oncol. 2016;27(4):559-74.
- Cunningham M, Iafolla M, Kanjanapan Y, et al. Evaluation of liver enzyme elevations and hepatotoxicity in patients treated with checkpoint inhibitor immunotherapy. PLoS One. 2021;16(6):e0253070.
- Santini FC, Rizvi H, Plodkowski AJ, et al. Safety and Efficacy of Re-treating with Immunotherapy after Immune-Related Adverse Events in Patients with NSCLC. Cancer Immunol Res. 2018;6(9):1093-1099.
- Pollack MH, Betof A, Dearden H, et al. Safety of resuming anti-PD-1 in patients with immune-related adverse events (irAEs) during combined anti-CTLA-4 and anti-PD1 in metastatic melanoma. Ann Oncol. 2018;29(1):250-255.
- Riveiro-Barciela M, Barreira-Díaz A, Callejo-Pérez A, et al. Retreatment With Immune Checkpoint Inhibitors After a Severe Immune-Related Hepatitis: Results From a Prospective Multicenter Study. Clin Gastroenterol Hepatol. 2023;21(3):732-740.
- Pro-Euro DILI-Network, “Consensus Conference on Drug-Induced Autoimmune Hepatitis (DI-AIH),” Malaga, Mar. 2022.







