Le attuali linee guida europee ed internazionali indicano i farmaci inibitori dell’integrasi (INSTI) come terapia antiretrovirale (ART) di prima scelta nelle persone che vivono con HIV (people living with HIV, PLWH) (1). Le strategie preferibili fra quelle contenenti INSTI, in un’ottica di moderna ART, sono quelle ad elevata barriera genetica e singola compressa quotidiana, caratterizzate da migliore accettabilità e facilità di assunzione rispetto a regimi multi-compressa. I regimi che rispondono a queste caratteristiche sono essenzialmente la triplice terapia (3DR) con bictegravir/emtricitabina/tenofovir alafenamide (B/F/TAF) e i regimi a due farmaci (2DR) con dolutegravir (DTG) associato a lamivudina (3TC) o rilpivirina (RPV). Lo switch a tali regimi si è rivelato sicuro ed efficace nel contesto di grandi trial clinici randomizzati.
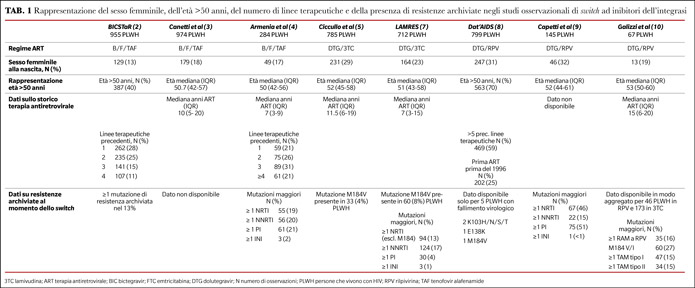
Se da un lato però il trial clinico è considerato il tipo di studio che consente di ottenere le migliori evidenze scientifiche, dall’altro, proprio a causa della necessità di eliminare gli effetti confondenti di particolari situazioni cliniche o terapie concomitanti alla ART, non sempre offre evidenze applicabili alla totalità delle PLWH. Il valore aggiunto degli studi osservazionali può quindi essere quello di fornire informazioni sulle popolazioni difficili da trattare, rappresentate in modo minoritario o non rappresentate nei grandi trial, come le PLWH con lunga storia di trattamento antiretrovirale e precedenti fallimenti virologici, con problematiche metaboliche o con età avanzata (Tabelle 1 e 2).
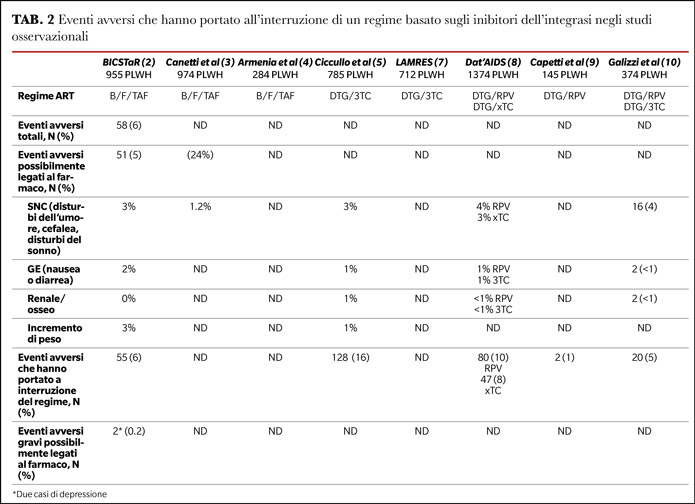
Studi osservazionali di switch a 3DR basati su inibitori dell’integrasi
I regimi a tre farmaci contenenti INSTI ad elevata barriera genetica e disponibili in singola compressa sono attualmente due, B/F/TAF e DTG/abacavir/3TC, quest’ultimo ormai poco utilizzato per l’aumentato rischio cardiovascolare correlato all’esposizione ad abacavir (1). Per quanto riguarda invece la terapia con B/F/TAF, questa costituisce ad oggi una scelta strategica adatta anche a popolazioni difficili da trattare, come dimostrato da diversi studi osservazionali che hanno coinvolto centinaia di persone con HIV.
Nello studio internazionale BICSTaR (2) sono state ad oggi incluse e seguite per 12 mesi 955 PLWH, che sono passate da un qualsiasi regime ART a B/F/TAF. I regimi di provenienza contenevano un INSTI nel 65% dei casi, ed il 92% delle PLWH arruolate aveva un HIV RNA < 50 copie/ml. Fra i partecipanti allo studio 129 (3.5%) erano donne e 387 (40.5%) avevano un’età superiore ai 50 anni.
Sia nella popolazione totale dello studio, che nelle donne e negli over 50, si sono confermate percentuali di soppressione virologica ad un anno superiori al 95%, con un numero di eventi avversi potenzialmente correlati al farmaco pari a 51 (5% dei partecipanti allo studio), percentuale molto contenuta tenendo conto che si tratta di uno studio di switch.
Il 3% dei partecipanti ha riportato un aumento del peso che è stato definito come evento non desiderato, tuttavia l’incremento ponderale medio è stato di 1 kg nei 12 mesi di osservazione, paragonabile a quello atteso nella popolazione generale. Inoltre si è registrato un significativo miglioramento della soddisfazione legata al trattamento ART riportata dai partecipanti dopo lo switch, con un’aderenza complessiva del 98%.
Dati simili di efficacia e tollerabilità sono stati evidenziati e confermati anche dallo studio di switch a B/F/TAF presentato da Canetti et al. allo IAS 2021 (3). In questo studio sono stati arruolati 974 partecipanti, tutti con HIV RNA inferiore alle 50 copie, il 66% dei quali proveniva da un regime basato su INSTI. A 12 mesi dallo switch è stato riscontrato un fallimento virologico in 18 casi, di cui 10 hanno nuovamente ottenuto la soppressione virologica continuando la terapia con B/F/TAF immodificata. Nessuno dei pazienti testati al fallimento ha sviluppato mutazioni di resistenza.
Per quanto riguarda invece lo studio della performance di B/F/TAF in PLWH con resistenze archiviate, i dati ci arrivano ancora una volta da uno studio italiano presentato da Armenia et al. all’ultima European AIDS Conference (4). In tale studio venivano descritte 284 PLWH che effettuavano uno switch con HIV RNA < 50 copie/ml, con almeno un test genotipico disponibile e con un’elevata prevalenza di resistenze archiviate. Di queste, 26/284 (9.2%) avevano una storia di ≥1 precedente fallimento virologico in corso di INSTI. A 60 settimane, la probabilità di blip o rebound virologico è stata calcolata del 9.7%, a seguito di 8 eventi di rebound e 16 blip virologici. Tuttavia, non è stata riscontrata nessuna associazione tra il rischio di blip/rebound e la storia di precedente fallimento virologico a INSTI e 5/8 PLWH con rebound virale hanno successivamente ottenuto una soppressione virologica senza necessità di variazioni della ART. Nessuno ha sviluppato resistenze emergenti nei confronti degli INSTI.
Studi osservazionali di switch a 2DR basati su inibitori dell’integrasi
Le due strategie di switch a 2DR supportate da maggiori evidenze scientifiche sono attualmente lo switch a DTG/3TC e a DTG/RPV. Per quanto riguarda lo switch a DTG/3TC, sono ormai disponibili i dati di studi osservazionali con follow-up fino a 5 anni (5,6).
In uno studio multicentrico condotto da Ciccullo et al. (5) sono state arruolate 785 PLWH, caratterizzate da una lunga storia di esposizione alla ART e da un’età mediana superiore ai 50 anni. L’incidenza di fallimento virologico è stata di 0.9 casi per 100 persone/anno, dopo un tempo mediano di 26 mesi dallo switch. Tutti i casi di fallimento hanno ottenuto in seguito una nuova soppressione della carica virale, in 8 casi proseguendo DTG/3TC, e nessuno ha sviluppato resistenze nei confronti di INSTI o NRTI, inclusi coloro che avevano la mutazione M184V al basale.
I fattori di rischio per il fallimento virologico sono risultati la storia di pregressi fallimenti e il sottotipo virale non-B, mentre la presenza della mutazione M184V è risultata un predittore di fallimento nei pazienti con viremia soppressa da meno di 88 mesi.
Altro studio con follow-up di 5 anni è stato condotto nella coorte prospettica SCOLTA, che ha confrontato i regimi 2DR e quelli 3DR contenenti il farmaco DTG (6). In questo studio i 2DR sono risultati protettivi nei confronti degli eventi avversi e caratterizzati da un maggior successo di durabilità rispetto ai 3DR.
Per quanto riguarda invece il ruolo delle resistenze archiviate in corso di DTG/3TC, lo studio multicentrico LAMRES, condotto in un contesto di real life, ha riscontrato come la mutazione M184V eserciti un impatto significativo in caso di soppressione virologica inferiore ai 3.5 anni al momento dello switch a DTG/3TC, fattore che tuttavia non si conferma statisticamente significativo dopo aggiustamento in analisi multivariata (7).
Per quanto riguarda invece lo switch a DTG/RPV, uno dei più grandi studi osservazionali disponibili è quello condotto nella coorte Dat’AIDS (8), che descrive i dati di 1374 PLWH che hanno effettuato uno switch a 2DR con DTG, di cui 799 con DTG/RPV. In questa coorte, dopo un tempo di osservazione mediano di 20 mesi, il fallimento virologico si è verificato in 30 PLWH (3.8%); fra esse, in due casi sono state evidenziate mutazioni emergenti al fallimento: la mutazione E138K in un caso, e le mutazioni E138K+K101E+N155H nel secondo caso.
I fattori di rischio identificati per il fallimento virologico sono risultati l’età inferiore ai 50 anni e la storia di un precedente fallimento a INSTI o NNRTI, quest’ultimo confermato anche in analisi multivariata.
Un altro interessante studio di switch a DTG/RPV è stato condotto da Capetti et al. (9) in una coorte di 145 PLWH seguite in diversi centri italiani di malattie infettive.
Tra queste, il 15% aveva HIV RNA ≥ 50 copie/ml al basale, e tutti hanno ottenuto una carica inferiore alle 50 copie a 96 settimane.
Infine, la performance dello switch a DTG/RPV nelle PLWH in soppressione virologica è stata confrontata con quella di DTG/3TC in uno studio italiano condotto da Galizzi et al. (10) e che ha coinvolto in totale 374 PLWH, di cui 67 in DTG/RPV. In questa coorte, l’incidenza cumulativa di fallimento virologico è stata di 3.3 e 1.57 per 100 persone/anno in DTG/3TC e DTG/RPV, rispettivamente. Nello studio è stato riscontrato che le PLWH che hanno sviluppato fallimento virologico avevano in media un più breve tempo di soppressione virologica rispetto alle altre (0.7 vs 1.5 anni), mentre l’impatto delle mutazioni archiviate o del sottotipo virale non è risultato significativamente associato al rischio di fallimento. In un solo caso è stata documentata una nuova mutazione a NRTI (M41L) emergente dopo fallimento a DTG/3TC.
In conclusione, i dati di real life sullo switch a B/F/TAF e a DTG associato a 3TC o RPV confermano i risultati di efficacia e sicurezza emersi dai clinical trial, anche in popolazioni difficili da trattare e con storia di lunga esposizione ai farmaci antiretrovirali e di ripetuti fallimenti virologici prima dello switch.
Il tempo di soppressione virologica prima del cambio terapeutico potrebbe essere un fattore di particolare importanza in quelle persone con resistenze archiviate che necessitino di uno switch a 2DR.
- EACS European Aids Clinical Society. Guidelines. Version 11.0. October 2021. https://www.eacsociety.org/media/final2021eacsguidelinesv11.0_oct2021.pdf.
- Mallolas J, Esposito V, Lambert J et al. Bictegravir/emtricitabine/tenofovir alafenamide (B/F/TAF) for the treatment of people living with HIV: 12-month effectiveness, persistence, and safety in a multi-country cohort study. EACS 2021, Poster PE2/57. https://europeanaidsconference.eacs.cyim.com/mediatheque/results.aspx?channel=28172&search=%7B%22Text%22%3A%22bicstar%22%7D&search_expr=bicstar.
- Canetti D, Poli, A, Galli, S et al. Switch to B/F/TAF in virally suppressed PLWH: efficacy and tolerability. vIAS 2021, PEB158. https://ias2021.org/wp-content/uploads/2021/07/IAS2021_Abstracts_web.pdf
- Armenia, D, Forbici, F, Bertoli, A et al. Virological response and resistance profile in virologically suppressed HIV-1 infected individuals switching to a bictegravir based treatment in clinical practice. EACS 2021, Oral BPD1/2. https://onlinelibrary.wiley.com/doi/full/10.1111/hiv.13183.
- Ciccullo A, Borghi V, Giacomelli A, et al. Five Years With Dolutegravir Plus Lamivudine as a Switch Strategy: Much More Than a Positive Finding. J Acquir Immune Defic Syndr. 2021;88(3):234–7.
- Taramasso L, De Vito A, Ricci ED, et al. Durability of Dolutegravir-Based Regimens: A 5-Year Prospective Observational Study. AIDS Patient Care STDS. 2021;35(9):342–53.
- Santoro MM, Armenia D, Teyssou E, et al. Virological efficacy of switch to DTG plus 3TC in a retrospective observational cohort of suppressed HIV-1 patients with or without past M184V - The LAMRES Study. J Glob Antimicrob Resist. 2022;S2213-7165(22)00189-8.
- Deschanvres C, Reynes J, Lamaury I, Rey D, et al. Dolutegravir-based dual maintenance regimens combined with lamivudine/emtricitabine or rilpivirine: risk of virological failure in a real-life setting. J Antimicrob Chemother. 2021;77(1):196–204.
- Capetti AF, Cossu MV, Sterrantino G, et al. Dolutegravir Plus Rilpivirine as a Switch Option in cART-Experienced Patients: 96-Week Data. Ann Pharmacother. 2018;52(8):740–6.
- Galizzi N, Poli A, Galli L, et al. Retrospective study on the outcome of two-drug regimens based on dolutegravir plus one reverse transcriptase inhibitor in virologically-suppressed HIV-infected patients. Int J Antimicrob Agents. 2020;55(3):105893.