Il carcinoma epatocellulare (HCC) è la quarta causa dimorte oncologica nel mondo e la principale causa di decesso dei pazienti con cirrosi compensata che ne rappresenta la principale condizione predisponente (1).
La sorveglianza del paziente a rischio di sviluppo di HCC, basata sull’ultrasononografia (US) ± dosaggio dell’alfa-fetoproteina sierica (AFP), è raccomandata da tutte le linee guida, in quanto essa incrementa le diagnosi precoci, l’accesso ai trattamenti curativi del tumore e la sopravvivenza dei pazienti rispetto alla diagnosi sintomatica, come chiaramente dimostrato da una meta-analisi includente >145.000 pazienti (2).
Fra i gruppi di pazienti meritevoli di sorveglianza le diverse linee guida includono i soggetti con epatopatia cronica da virus B (HBV) o virus C (HCV) dell’epatite, seppure con alcune differenze riguardo alle loro caratteristiche (3-5) (Tabella 1). In particolare, le linee guida europee raccomandano la sorveglianza convenzionale (US±AFP semestrale) per i pazienti con cirrosi o epatite cronica HBV-relata che raggiungono un punteggio ≥10 secondo il calcolatore di rischio PAGE-B, e per quelli con cirrosi HCV-relata, mentre suggeriscono che la procedura può essere considerata in caso di epatite cronica e fibrosi F3 secondo Metavir (3). Tali precisazioni sono rese necessarie dalla consapevolezza che il rapporto costo-efficacia e il rischio-beneficio di questa procedura dipendono, oltre che dal guadagno di sopravvivenza ottenibile con la terapia oncologica, dall’entità del rischio di HCC (6,7).

Nella decisione di implementare la sorveglianza vannoperò considerati anche i suoi aspetti negativi ed i rischi, riconducibili ai costi a carico del sistema sanitario e del paziente (assenze dal lavoro, viaggi per raggiungere la sede di esecuzione delle indagini), al rischio di sovra-diagnosi (identificazione di una patologia che non influenzerà significativamente la sopravvivenza), ai risultati falsi positivi (con inutile esposizione ad accertamenti confermativi, quali TC, RMN e biopsia) e falsi negativi (con conseguente diagnosi ritardata), nonché ai riflessi psicologici negativi (stress, depressione) derivanti dalla consapevolezza da parte del paziente di essere a rischio neoplastico (7).
Considerato ciò, nella decisione di implementare una sorveglianza deve entrare in gioco anche la consapevolezza che il controllo virologico (viremia non dosabile) dell’infezione HBV (grazie ai farmaci nucleo(t)sidici) e l’eradicazione dell’infezione HCV (grazie agli antivirali diretti), ottenibili nella quasi totalità dei soggetti trattati, comportano una sostanziale riduzione – seppure non l’azzeramento – del rischio di HCC rispetto ai casi non trattati o resistenti al trattamento (8-10). Poiché nei Paesi con elevato prodotto interno lordo pressoché tutti i pazienti con riconosciuta infezione cronica da HBV o HCV vengono oggi avviati a terapia antivirale, i casi in controllo virologico o guariti stanno rapidamente aumentando, sopravanzando i soggetti viremici. A tal proposito, è stato previsto che, negli Stati Uniti, la percentuale dei soggetti guariti dall’infezione HCV salirà dai 106.000 casi del 2012 a 649.000 casi nel 2030 e, fra i candidati alla sorveglianza, la percentuale di questi casi aumenterà dall’8.5% al 64.6% (11). Stante tale evoluzione epidemiologica della malattia epatica virale e considerato che il rischio di HCC è un determinante chiave della costo-efficacia della sorveglianza, si pone quindi il problema se e come sorvegliare questi pazienti. Le attuali linee guida sono piuttosto elusive (e talora discordanti) in merito a tale problema, lasciando un ampio spazio alle discrezionalità riguardo ai pazienti non cirrotici.
Va poi ricordato che l’US è una metodica fortemente operatore-dipendente, con una sub-ottimale sensibilità (≃50%) per lesioni <2 cm e che l’aggiunta dell’AFP aumenta tale sensibilità al 63%, riducendo però la specificità dello screening (12). Di contro, l’impiego routinario di TC e RMN è improponibile per gli alti costi, l’insufficiente disponibilità di attrezzature ed i rischi connessi (esposizione a radiazioni, reazioni avverse a mezzi di contrasto).
Un ulteriore limite di qualsiasi sorveglianza che preveda l’accesso a strutture qualificate per l’accertamento strumentale sta nell’insoddisfacente tasso di adesione del paziente al programma, problema particolarmente evidente nei pazienti guariti dall’infezione o in controllo virologico, che rappresentano condizioni rassicuranti in termini di prognosi della malattia epatica. Ciò è ben dimostrato dal progressivo declino della percentuale di coloro che si attengono al programma di visite dopo avere ottenuto la guarigione dell’infezione HCV (13).
Per ovviare ai suddetti limiti della sorveglianza convenzionale sono allo studio due strategie operanti su versanti diversi:
- l’impiego di combinazioni di biomarcatori sierici, quali il GALAD (Gender, Age, Lectin-bound AFP, AFP, Des-carboxy-prothrombin) e derivati (14), che eviterebbero l’accesso ai centri ecografici ed eliminerebbero la soggettività del risultato dell’US
- l’impiego, nei pazienti a più elevato rischio di HCC, della RMN abbreviata (AMRI), che riduce nettamente il tempo di esecuzione rispetto all’indagine convenzionale pur mantenendo un’eccellente accuratezza diagnostica per piccole lesioni (15). In uno studio retrospettivo, l’AMRI è risultata costo-efficace nei pazienti con un rischio annuo di HCC >3% (16).
Entrambe le soluzioni, se validate in studi di fase III (o meglio IV), potrebbero trovare un’applicabilità routinaria in determinate fasce di pazienti, con un rapporto costo-efficacia migliore di quello della sorveglianza convenzionale (17).
Sulla base di un Rapporto Incrementale di Costo-Efficacia (ICER) = $50.000/anno guadagnato di qualità di vita (QALY), l’incidenza annuale minima di HCC necessaria per implementare una sorveglianza convenzionale costo-efficace è 1.3%, e si abbassa allo 0.82% qualora la periodicità della procedura divenga annuale (18). Degno di attenzione è il fatto che una rilevante percentuale (fino al 70%) di pazienti guariti dall’infezione HCV o con infezione HBV sotto controllo non raggiunge tali soglie (19). Va però considerato che orientamenti moderni propongono di incrementare la disponibilità a pagare (willingness-to-pay) fino a $150.000/QALY, evenienza che abbassa la soglia di costo-efficacia allo 0,40% di incidenza tumorale annua (20). Utilizzando queste soglie ribassate, una percentuale decisamente maggiore di pazienti virologici trattati con antivirali rientrerebbe fra coloro per i quali la procedura viene considerata costo-efficace, seppure a fronte di una spesa decisamente maggiore per QALY guadagnato. In ultima analisi, questi modelli di economia sanitaria forniscono le coordinate per scelte gestionali che tengano conto delle risorse economiche dei diversi sistemi sanitari.
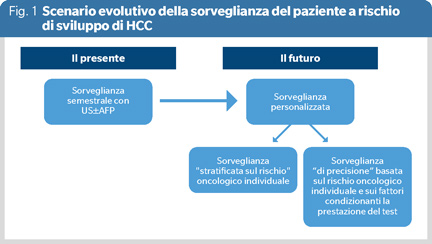 A fronte di ciò e in una prospettiva di costo-efficacia e rischio-beneficio, si può assumere che il futuro richiederà l’implementazione di programmi di sorveglianza che non propongano lo stesso vestito per tutte le taglie, ma risultino personalizzati, basandosi quantomeno sull’entità del rischio oncologico individuale (sorveglianza rischio-stratificata) o che considerino, oltre al rischio, anche i principali fattori (sesso, etnia, eziologia, fenotipo) capaci di influenzare la prestazione del test di screening (sorveglianza di precisione) (Figura 1), al fine di:
A fronte di ciò e in una prospettiva di costo-efficacia e rischio-beneficio, si può assumere che il futuro richiederà l’implementazione di programmi di sorveglianza che non propongano lo stesso vestito per tutte le taglie, ma risultino personalizzati, basandosi quantomeno sull’entità del rischio oncologico individuale (sorveglianza rischio-stratificata) o che considerino, oltre al rischio, anche i principali fattori (sesso, etnia, eziologia, fenotipo) capaci di influenzare la prestazione del test di screening (sorveglianza di precisione) (Figura 1), al fine di:
- ridurre l’uso di risorse di scarsa utilità e l’esposizione ai rischi della metodica nei pazienti a basso rischio oncologico
- migliorare il tasso di identificazione del tumore in fase precoce
- mantenere un sostenibile rapporto di costo-efficacia (17).
Allo scopo, la scelta del test e dell’intervallo con cui ripeterlo non può prescindere da una precisa conoscenza del rischio oncologico individuale fornita da affidabili calcolatori. Oggi disponiamo di numerosi calcolatori validati, alcuni dei quali generalisti, cioè sganciati dall’eziologia della malattia epatica, altri specifici per eziologia (anche dopo cura o controllo dell’infezione). Per una dettagliata descrizione di questi calcolatori e delle loro prestazioni si rimanda ad un articolo dedicato all’argomento (19).
La figura 2 riporta una proposta di sorveglianza personalizzata, basata sul rischio oncologico e costruita tenendo conto dei dati di costo-efficacia delle diverse metodiche di screening, assumendo che:
- un’incidenza annua di HCC <0.6-0.8% non giustifichi la procedura
- periodicità più stringenti e test più costosi, ma più efficienti, possano diventare accettabili nei pazienti a più alto rischio oncologico, riducendosi il numero di individui da sorvegliare per identificare un tumore (number needed to survey).
Adottando tale strategia, fino al 70% dei pazienti con malattia virale soppressa o guarita non entrerebbe nei programmi di sorveglianza, evitando loro i rischi fisici e psicologici della procedura e liberando ingenti risorse economiche per più fruttuosi scopi assistenziali.
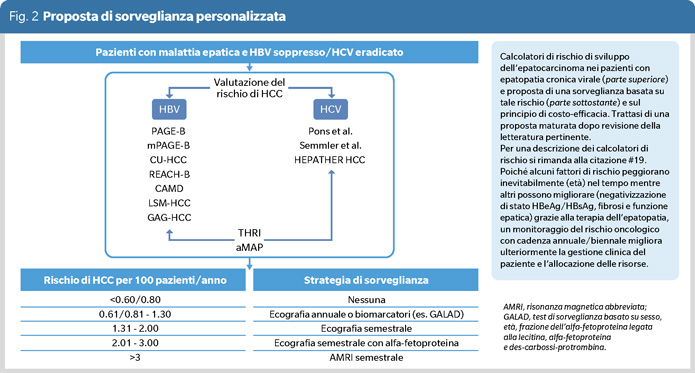
Ovviamente, la proposta e le soglie di stratificazione indicate vanno adattate alle risorse economico-assistenziali locali, altamente variabili fra le diverse aree geo-politiche.
Aspetti priincipali
- La sorveglianza del paziente a rischio di HCC oggi si basa sulla ripetizione semestrale dell’ultrasonografia (US) epatica ± il dosaggio dell’alfa-fetoproteina
- La sorveglianza ha costi, aspetti negativi e rischi per il paziente
- Il suo rapporto costo-efficacia dipende da: entità del rischio oncologico, prestazioni del test e guadagno di vita ottenibile con la terapia oncologica. Proporre la stessa sorveglianza a pazienti con rischio oncologico diverso non è la strategia ottimale
- La guarigione dell’infezione HCV ed il controllo dell’infezione HBV comportano una riduzione (ma non l’annullamento) del rischio di HCC, cosicché una rilevante percentuale di questi soggetti non risulterebbe candidabile ad una sorveglianza convenzionale costo-efficace
- Una sorveglianza personalizzata, stratificata sul rischio oncologico e non necessariamente basata sull’US, rappresenta il futuro di questa pratica
- Singal AG, Kanwal F, Lloved JM. Global trends in hepatocellular carcinoma epidemiology: implications for screening, prevention and therapy. Nat Rev Clin Oncol 2023;20:864-884.
- Singal AG, Zhang E, Narasimman M, et al. HCC surveillance improves early detection, curative treatment receipt, and survival in patients with cirrhosis: A meta-analysis. J Hepatol 2022;77(1):128-39.
- Galle PR, Forner A, Llovet JM, et al. EASL Clinical Practice Guidelines: Management of hepatocellular carcinoma. J Hepatol 2018;69(1):182–236.
- Singal AG, Llovet JM, Yarchoan M, et al. AASLD practice guidance on prevention, diagnosis, and treatment of hepatocellular carcinoma. Hepatology 2023;78(6):1922-1965.
- Omata M, Cheng AL, Kokudo N, et al. Asia-Pacific clinical practice guidelines on the management of hepatocellular carcinoma: a 2017 update. Hepatol Int 2017;11(4):317-70.
- Goossens N, Singal AG, King LY, et al. Cost-Effectiveness of risk score-stratified hepatocellular carcinoma screening in patients with cirrhosis. Clin Transl Gastroenterol 2017;8(6):e101
- Singal AG, Patibandla S, Obi J, et al. Benefits and harms of hepatocellular carcinoma surveillance in a prospective cohort of patients with cirrhosis. Clin Gastroenterol Hepatol 2021;19(9):1925-1932.e1
- Papatheodoridis GV, Idilman R, Dalekos GN, et al. The risk of hepatocellular carcinoma decreases after the first 5 years of entecavir or tenofovir in Caucasians with chronic hepatitis B. Hepatology; 66(5):1444-1453.
- Carrat F, Fontaine H, Dorival C, et al. Clinical outcomes in patients with chronic hepatitis C after direct-acting antiviral treatment: a prospective cohort study. Lancet 2019;393(10179):1453-1464.
- Lockart I, Yeo MGH, Hajarizadeh B, et al. HCC incidence after hepatitis C cure among patients with advanced fibrosis or cirrhosis: A metaanalysis. Hepatology 2022;76(1):139-154.
- Chen Q , Ayer T, Adee MG, et al. Assessment of incidence of and surveillance burden for hepatocellular carcinoma among patients with hepatitis C in the era of Direct-Acting Antiviral agents. JAMA Netw Open 2020;3(11):e2021173.
- Tzartzeva K, Obi J, Rich NE, et al. Surveillance Imaging and alpha-fetoprotein for early detection of hepatocellular carcinoma in Patients with cirrhosis: a meta-analysis. Gastroenterology 2018;154(6):1706-1718.e1.
- Toyoda H, Yasuda S, Shiota S, et al. Adherence to regular surveillance visits for hepatocellular carcinoma in patients with chronic hepatitis C virus infection who achieved sustained virologic response. Eur J Gastroenterol Hepatol 2022;34(6):693-697.
- Berhane S, Toyoda H, Tada T, et al. Role of the GALAD and BALAD-2 serologic models in diagnosis of hepatocellular carcinoma and prediction of survival in patients. Clin Gastroenterol Hepatol 2016;14(6):875-886.e6.
- Gupta P, Soundararajan R, Patel A, et al. Abbreviated MRI for hepatocellular carcinoma screening: A systematic review and meta-analysis. J Hepatol 2021;75(1):108-119.
- Nahon P, Najean M, Layese R, et al. Early hepatocellular carcinoma detection using magnetic resonance imaging is cost-effective in high-risk patients with cirrhosis. JHEP Reports 2022;4(1):100390.
- Kao S-YZ, Sangha K, Fujiwara N, et al. Cost-effectiveness of a precision hepatocellular carcinoma surveillance strategy in patients with cirrhosis. eClinicalMedicine 2024;75:102755.
- Farhang Zangneh H, Wong WWL, Sander B, et al. Cost effectiveness of hepatocellular carcinoma surveillance after a Sustained Virologic Response to therapy in patients with hepatitis C virus infection and advanced fibrosis. Clin Gastroenterol Hepatol 2019;1 13:376-388.
- Lani L, Stefanini B, Trevisani F. Surveillance for Hepatocellular Carcinoma in Patients with Successfully Treated Viral Disease of the Liver: A systematic review. Liver Cancer 2024;7(9):1840-1849.e16.
- Chhatwal J, Hajjar A, Mueller PP, et al. Hepatocellular carcinoma incidence threshold in virologically cured hepatitis C individuals. Clin Gastroenterol Hepatol 2024;22:91-101







