Candida parapsilosis (CP) fu descritta nel 1928 da Ashford, che isolò una specie di Monilia dalle feci, osservandone l’incapacità di fermentare il maltosio. Per distinguerla dalla più comune Monilia psilosis - poi identificata come Candida albicans - Ashford coniò il termine parapsilosis. Fino agli anni ’40, CP era considerata non patogena, finché non fu documentato un caso fatale di endocardite in un tossicodipendente, ipotizzando un’infezione facilitata dall’introduzione esogena del microrganismo tramite iniezioni endovenose. Queste osservazioni anticiparono il ruolo di CP nelle infezioni associate a dispositivi invasivi e soluzioni parenterali (1).
Questo articolo presenta una revisione su CP, con focus sugli aspetti clinici e sull’evoluzione della resistenza agli antifungini.
Epidemiologia
Storicamente, C. albicans era la principale causa di infezioni da Candida. Negli ultimi anni, tuttavia, le infezioni da specie non-albicans, come C. glabrata, CP e C. tropicalis, sono aumentate, riducendo la prevalenza globale di C. albicans a meno del 50% (2). CP è oggi la seconda o terza causa più comune di candidiasi invasiva, con tassi di prevalenza variabili per regione geografica e popolazione a rischio. In particolare, CP è più frequente nei Paesi del Mediterraneo europeo, inclusa l’Italia (16-41.0%), in Sud America (25.3-38.5%), in Asia (18.8-27.1%) e in Medio Oriente (11.4-34.7%). Nell’Europa centrale e settentrionale predomina C. glabrata. Le cause di tali differenze geografiche restano poco chiare (2).
Patogenesi delle infezioni
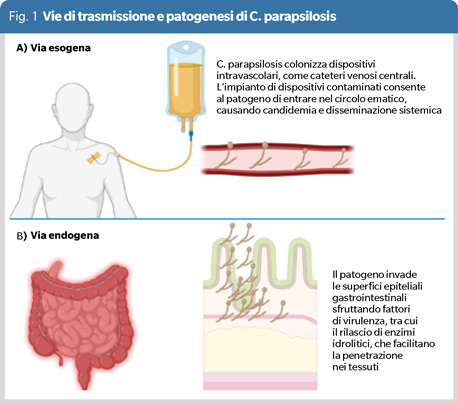 Le specie di Candida possono causare infezioni invasive attraverso due meccanismi principali (Figura 1). Il primo è la via endogena, ossia la traslocazione delle specie attraverso la mucosa gastrointestinale, predominante nei pazienti neutropenici sottoposti a chemioterapia, dove le mucositi facilitano l’ingresso del patogeno nel sangue. Il secondo è la via esogena, che coinvolge la colonizzazione di dispositivi intravascolari, come cateteri venosi centrali (CVC), favorendo lo sviluppo di candidemia (2). Nel caso di CP, studi murini mostrano una minore capacità di traslocazione gastrointestinale rispetto ad altre specie, con una ridotta probabilità di traslocazione endogena (2). La trasmissione nosocomiale per via esogena (da paziente a paziente, da operatori sanitari o superfici inerti) sembra essere il meccanismo principale. Studi di genotipizzazione hanno infatti, evidenziato una forte somiglianza genetica tra isolati ospedalieri e ceppi infettivi, associando CP a cluster epidemici (2).
Le specie di Candida possono causare infezioni invasive attraverso due meccanismi principali (Figura 1). Il primo è la via endogena, ossia la traslocazione delle specie attraverso la mucosa gastrointestinale, predominante nei pazienti neutropenici sottoposti a chemioterapia, dove le mucositi facilitano l’ingresso del patogeno nel sangue. Il secondo è la via esogena, che coinvolge la colonizzazione di dispositivi intravascolari, come cateteri venosi centrali (CVC), favorendo lo sviluppo di candidemia (2). Nel caso di CP, studi murini mostrano una minore capacità di traslocazione gastrointestinale rispetto ad altre specie, con una ridotta probabilità di traslocazione endogena (2). La trasmissione nosocomiale per via esogena (da paziente a paziente, da operatori sanitari o superfici inerti) sembra essere il meccanismo principale. Studi di genotipizzazione hanno infatti, evidenziato una forte somiglianza genetica tra isolati ospedalieri e ceppi infettivi, associando CP a cluster epidemici (2).
Un aspetto cruciale della patogenicità di CP è la capacità di colonizzare rapidamente gli ambienti ospedalieri e le mani degli operatori sanitari, oltre a formare biofilm su dispositivi medici come i CVC. La proliferazione del microrganismo in soluzioni oleose per nutrizione parenterale totale è un noto fattore di rischio per adulti malnutriti e neonati a basso peso in terapia intensiva (2). Questi meccanismi sottolineano l’importanza di strategie mirate per prevenire le infezioni da CP, con enfasi su igiene delle mani, sanificazione ospedaliera e gestione dei dispositivi invasivi
Manifestazioni cliniche
Le infezioni da CP presentano manifestazioni cliniche simili a quelle causate da altre specie di Candida. Sebbene segni e sintomi varino in base alla popolazione a rischio, una presentazione comune è rappresentata da sepsi o shock settico, difficilmente distinguibili da condizioni batteriche analoghe (3).
Nonostante la somiglianza clinica, alcune peculiarità, tuttavia, distinguono le infezioni da CP da quelle da C. albicans. Studi epidemiologici, tra cui uno condotto in Spagna, hanno identificato fattori predittivi indipendenti per CP: età neonatale, trapianto d’organo solido, precedente terapia antifungina (soprattutto fluconazolo) e uso di nutrizione parenterale (4). Inoltre, la presenza di un CVC rappresenta un ulteriore fattore di rischio (5). CP è stata isolata nel 27% delle emocolture positive (6), ma solo nel 2.6% dei campioni intra-addominali, suggerendo una predilezione per candidemie associate a dispositivi intravascolari (5).
In termini di mortalità, i pazienti con infezioni da CP mostrano tassi inferiori rispetto a C. albicans (7% contro 56% entro 7 giorni), coerenti con la minore virulenza di CP, evidenziata anche in modelli animali (7).
Evoluzione della resistenza a fluconazolo
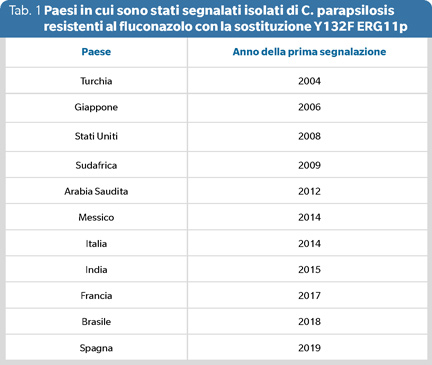 Tradizionalmente, CP era ritenuta sensibile al fluconazolo, con tassi di resistenza inferiori al 5% fino al 2016. Tuttavia, recenti studi hanno evidenziato un incremento della resistenza al fluconazolo in CP, con tassi significativamente più elevati: 9.2% in Francia, 26.4% in Turchia, 33% in Italia, 54% in Messico, 67.9% in Brasile e 78% in Sudafrica (8,9). Il principale meccanismo di resistenza in CP è la sostituzione dell’aminoacido Y132F nella proteina ERG11p, spesso associata a resistenza crociata al voriconazolo, posaconazolo e isavuconazolo (9). Questo fenomeno, progressivamente osservato in diverse regioni geografiche nel corso degli ultimi anni (Tabella 1), rappresenta una sfida terapeutica per due motivi principali.
Tradizionalmente, CP era ritenuta sensibile al fluconazolo, con tassi di resistenza inferiori al 5% fino al 2016. Tuttavia, recenti studi hanno evidenziato un incremento della resistenza al fluconazolo in CP, con tassi significativamente più elevati: 9.2% in Francia, 26.4% in Turchia, 33% in Italia, 54% in Messico, 67.9% in Brasile e 78% in Sudafrica (8,9). Il principale meccanismo di resistenza in CP è la sostituzione dell’aminoacido Y132F nella proteina ERG11p, spesso associata a resistenza crociata al voriconazolo, posaconazolo e isavuconazolo (9). Questo fenomeno, progressivamente osservato in diverse regioni geografiche nel corso degli ultimi anni (Tabella 1), rappresenta una sfida terapeutica per due motivi principali.
Il primo è la riduzione delle opzioni terapeutiche, aggravata dalla scarsa sensibilità di CP alle echinocandine in vitro (8). Il secondo è la capacità di generare cluster nosocomiali che, a differenza di C. albicans, coinvolgono più pazienti, possono persistere per anni negli ospedali e diventare endemici, con un comportamento simile a C. auris (8). La descrizione clinica dei pazienti con infezioni da C. parapsilosis resistente al fluconazolo (CP-R-FLZ) è limitata. Studi comparativi con CP sensibile al fluconazolo (CP-S-FLZ) non hanno rilevato differenze significative nella presentazione clinica o nei fattori di rischio, però molti pazienti con CP-R-FLZ erano ricoverati in terapia intensiva, il che evidenzia il ruolo di questi ambienti nella diffusione dell’infezione. Interessante è la bassa percentuale (<20%) di pazienti con CP-R-FLZ che avevano ricevuto fluconazolo: circostanza che suggerisce che la trasmissione nosocomiale è il principale motore della resistenza (9).
La mortalità associata a fungemie da CP-R-FLZ varia dal 9% al 78%, con risultati contrastanti (9). Alcuni studi indicano una maggiore mortalità associata alla resistenza, mentre altri non rilevano differenze, probabilmente per limiti metodologici come piccoli campioni e bias di selezione. Recentemente abbiamo condotto uno studio retrospettivo multicentrico (2018-2022) su 457 pazienti adulti con emocolture positive per CP trattati con terapia appropriata (fluconazolo o echinocandine) (10). Di questi, 42.9% avevano CP-R-FLZ e 57.1% CP-S-FLZ. La mortalità a 30 giorni era simile: 28.6% per CP-R-FLZ e 28.4% per CP-S-FLZ. Fattori associati a maggiore mortalità includevano età avanzata, tumori solidi, precedente uso di antifungini e shock settico, mentre né la resistenza né la terapia iniziale mostravano correlazione significativa. Tuttavia, nei pazienti con CP-R-FLZ è stato osservato un rischio maggiore di recidiva a un anno, il che richiede la necessità di portare avanti ulteriori studi (10).
Conclusioni
CP rappresenta una seria minaccia per la salute pubblica, strettamente legata alla trasmissione nosocomiale. Le principali problematiche includono la formazione di biofilm su dispositivi medici, la gestione complessa dei focolai clonali e la crescente resistenza agli azoli. Sebbene questa resistenza non sembri influire sulla mortalità con trattamenti adeguati, è associata a un maggior rischio di recidive e a un potenziale impatto su costi sanitari, ricoveri prolungati e disabilità.
Misure preventive per il controllo delle infezioni rimangono essenziali per limitare la diffusione. L’esperienza con C. auris può offrire spunti preziosi per affrontare questa sfidaemergente, ma sono necessari ulteriori studi per valutare l’efficacia delle politiche di controllo e sviluppare strumenti diagnostici rapidi e accurati per l’identificazione e la genotipizzazione degli isolati nella pratica microbiologica quotidiana.
- Weems JJ, Jr. Candida parapsilosis: epidemiology, pathogenicity, clinical manifestations, and antimicrobial susceptibility. Clin Infect Dis. 1992;14(3):756-66.
- Toth R, Nosek J, Mora-Montes HM, et al. Candida parapsilosis: from Genes to the Bedside. Clin Microbiol Rev. 2019;32(2).
- King J, Pana ZD, Lehrnbecher T, et al. Recognition and Clinical Presentation of Invasive Fungal Disease in Neonates and Children. J Pediatric Infect Dis Soc. 2017;6(suppl_1):S12-S21.
- Rodriguez D, Almirante B, Cuenca-Estrella M, et al. Predictors of candidaemia caused by non-albicans Candida species: results of a population based surveillance in Barcelona, Spain. Clin Microbiol Infect. 2010;16(11):1676-82.
- Puig-Asensio M, Padilla B, Garnacho-Montero J, et al. Epidemiology and predictive factors for early and late mortality in Candida bloodstream infections: a population-based surveillance in Spain. Clin Microbiol Infect. 2014;20(4):O245-54.
- Diaz-Garcia J, Mesquida A, Gomez A, et al. Antifungal Susceptibility Testing Identifies the Abdominal Cavity as a Source of Candida glabrata-Resistant Isolates. Antimicrob Agents Chemother. 2021;65(12):e0124921.
- Puig-Asensio M, Peman J, Zaragoza R, et al. Impact of therapeutic strategies on the prognosis of candidemia in the ICU. Crit Care Med. 2014;42(6):1423-32.
- Daneshnia F, de Almeida Junior JN, Ilkit M, et al. Worldwide emergence of fluconazole-resistant Candida parapsilosis: current framework and future research roadmap. Lancet Microbe. 2023;4(6):e470-e80.
- Escribano P, Guinea J. Fluconazole-resistant Candida parapsilosis: A new emerging threat in the fungi arena. Front Fungal Biol. 2022;3:1010782.
- Vena A, Tiseo G, Falcone M et al. Impact of Fluconazole Resistance on the Outcomes of Patients With Candida parapsilosis Bloodstream Infections: A Retrospective Multicenter Study. Clin Inf Dis 2024;On Press.







