I progressi nelle terapie antiretrovirali (ART) hanno guidato il cambiamento nella storia naturale dell’HIV e sono stati paralleli a altrettanti cambiamenti antropometrici che si sono manifestati nelle persone che vivono con l’HIV (PWH). In dettaglio, la wasting syndrome è stata descritta nel periodo pre-ART, la lipoatrofia nel periodo pre-ART, la lipoipertrofia nel periodo late-ART (1).
I regimi di terapia attualmente utilizzati basati sugli inibitori dell’integrasi (INSTI), non sono esenti da possibili cambiamenti di composizione corporea e nonostante abbiamo un impatto sostanzialmente nullo sul metabolismo lipidico, sono stati associati all’aumento di peso, sia nelle PWH naïve che in quelle experienced, generando il timore di un’epidemia di obesità (1-4).
In questo contesto, gli studi sull’aumento di peso dimostrano che i cambiamenti nella composizione corporea sono al crocevia di molti percorsi metabolici quali l’insulino-resistenza, la steatosi epatica, le malattie cardio e cerebrovascolari ecc. Inoltre, i farmaci che inducono o piuttosto prevengono l’obesità sono di fondamentale importanza nelle persone con HIV non appena associati a un appropriato intervento sullo stile di vita. Lo studio PASO DOBLE si inserisce in questo ampio contesto scientifico e avendo caratteristiche metodologiche di rilievo offre dati robusti con potenziali ricadute assistenziali che meritano una ampia discussione.
PASO DOBLE (NCT04884139) è uno studio clinico randomizzato multicentrico in aperto, di fase IV che valuta l’efficacia di DTG/3TC rispetto a BIC/FTC/TAF per il mantenimento della soppressione virologica nelle PWH, condotto in 30 centri clinici spagnoli (Figura 1). Lo studio è stato presentato al congresso IAS di Monaco e non è ancora stato pubblicato. Ha ricevuto un finanziamento incondizionato da VIIV (5).
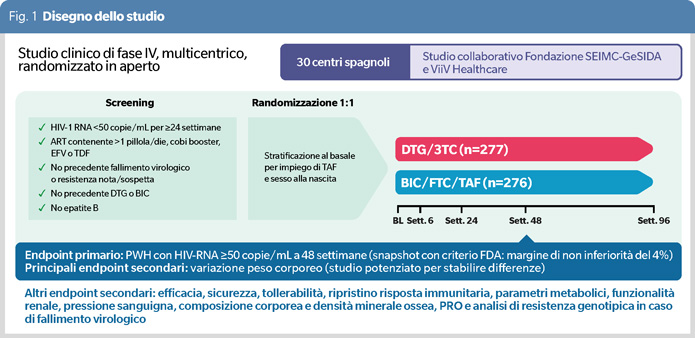
Questo studio oltre alle variabili viro-immunologiche, offre un focus particolare sull’impatto dello switch sulle variabili metaboliche e antropometriche della popolazione studiata. Grazie a una serie di sotto-studi saranno poi disponibili dati di lipidomica, e studi meccanicistici sulla senescenza del tessuto adiposo e sulla steatosi epatica. Non possiamo che congratularci rispetto alla capacità di networking dei centri clinici spagnoli (attraverso una collaborazione tra la Fondazione SEIMC - GeSIDA) che sono stati in grado di costruire una rete collaborativa paragonabile al sistema ACTG statunitense.
Gli elementi di rigore metodologico
Lo studio mostra alcuni elementi di grande rigore metodologico (Figura 1), ricordiamo:
- La popolazione dello studio è rappresentativa delle coorti HIV dell’Europa occidentale compreso la presenza di un 27% di donne e una proporzione significativa di pazienti sovrappeso o obesi (33% e 17% rispettivamente).
- Tutti i pazienti dello studio non erano mai stati esposti in precedenza ai due inibitori dell’integrasi oggetto dello studio rispettivamente bictegravir e dolutegravir permettendo un confronto testa a testa.
- I pazienti provenivano da regimi multi-compressa o con booster, o regimi con TDF o EFV, o più in generale da regimi più complessi o potenzialmente che usavano farmaci meno sicuri.
- La randomizzazione era stratificata per sesso e per uso al baseline di TAF per evitare l’impatto di quest’ultimo sulle variabili antropometriche prima del cambiamento terapeutico.
- La dimensione campionaria è stata calcolata sulla possibilità di rilevare una differenza di cambiamento di peso significativa tra i due bracci.
L’endpoint primario era la percentuale di PWH con RNA ≥50 copie/mL a 48 settimane (snapshot con criterio FDA che prevede un margine di non inferiorità del 4%) nella popolazione esposta secondo intention-to-treat. Gli outcome secondari erano l’aumento di peso assoluto, la variazione del BMI e la percentuale di partecipanti con variazione di peso superiore al 5%.
Complessivamente tra luglio 2021 e marzo 2023, sono stati arruolati 553 PWH, che hanno iniziato rispettivamente DTG/3TC (n=277) o BIC/FTC/TAF (n=276), di cui 155 (28%) con TAF nel regime precedente. Rispetto all’outcome primario, a 48 settimane, DTG/3TC è risultato non inferiore a BIC/FTC/TAF [differenza di rischio tra DTG/3TC (2.2%) vs BIC/FTC/TAF (0.7%) 1.4%, IC 95% -0.5–3.4]. I dati virologici non hanno bisogno di commenti, essendo stato raggiunto il risultato atteso di non inferiorità virologica tra i due regimi ed essendoci stato un unico fallimento nel braccio BIC/FTC/TAF e nessuna insorgenza di mutazioni di resistenza. Il profilo di tollerabilità di entrambi i regimi è stato ottimo. Ci sono state pochissime interruzioni (DTG/3TC=1, 0.4%; BIC/FTC/TAF=2, 0.7%) dovute a eventi avversi (5).
Le variazioni di peso corporeo
Il risultato più rilevante di PASO DOBLE è quello relativo alle variazioni di peso registrate nei due bracci. Il peso medio è stato aggiustato per peso la baseline, sesso, presenza di TAF nel trattamento precedente, età ed etnia. Si è osservato un aumento di peso significativamente maggiore con BIC/FTC/TAF (1.81 kg, IC 95% 1.28-2.34) rispetto a DTG/3TC (0.89 kg, IC 95% 0.37-1.41), dimostrando una differenza tra i bracci di 0.92 kg, IC 95% 0.17-1.66 (5).
Non è però questo piccolo scarto di peso il parametro clinicamente più significativo, che invece è rappresentato dalla percentuale di partecipanti con aumento di peso >5% a 48 settimane. Questa scelta, per quanto arbitraria, per ammissione del professor Esteban Martinez, ricercatore principale dello studio, deriva da una ricerca italiana che ha documentato che questa percentuale di incremento ponderale corrisponde al rischio di insorgenza di insulino-resistenza in persone senza precedente danno metabolico (6). PASO DOBLE ha documentato un aumento dell’81% di probabilità di incremento di peso clinicamente significativo che si è verificato nel 29.9% nei pazienti trattati con BIC/FTC/TAF e del 20% nei pazienti trattati con DTG/3TC (OR aggiustato 1.81, IC 95% 1.19-2.76) (Figura 2) (5). Inoltre, è importante sottolineare che circa il 10% della popolazione studiata in entrambi i gruppi ha sperimentato una perdita di peso superiore al 5%, suggerendo che il trattamento antiretrovirale può essere associato anche al miglioramento della salute metabolica della persona con l’HIV.
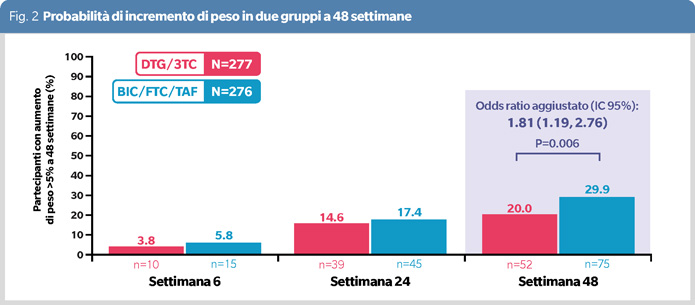
Nel braccio BIC/FTC/TAF, l’aumento di peso sembrava essere guidato non solo dall’aggiunta del TAF, ma anche dall’esposizione a TDF, ABC o NNRTI nel regime precedente allo switch. In particolare, se il regime precedente comprendeva ABC l’incremento significativo di peso era del 30.6% mentre se comprendeva TDF era del 40.7%, indicando un effetto additivo indotto da TAF in combinazione a un farmaco che riduce il peso (TDF o ABC o EFV) nel regime precedente. L’impatto del backbone nucleosidico non era invece presente nei pazienti randomizzati a DTG/3TC (5).
La variazione di peso nelle donne (OR 1.131, IC 95%: 0.700-1.826) non differiva da quella negli uomini, sottolineando la non trasferibilità nella casistica europea dei risultati dello studio ADVANCE che mostravano la popolazione femminile come maggiormente esposta al rischio di incremento di peso.
Il concetto di salute metabolica
PASO DOBLE, concentrandosi sull’outcome antropometrico offre spunti di riflessione sul concetto di salute metabolica che negli ultimi anni si è venuto ad affermare come costrutto positivo che, pur considerando ancora variabili metaboliche che condividono complessi meccanismi patofisiologici, offre un modello di cura incentrato sul paziente (7). La salute metabolica è una tabella di marcia che dovrebbe accompagnare gli individui nel corso della vita e nella storia naturale delle malattie croniche. Nell’ambito dell’HIV, questo approccio è particolarmente rilevante in quanto si adatta alla relazione tra infezione virale cronica, esposizione all’ART e l’individuo nel suo ambiente. Sia storicamente (passando dall’era pre-ART all’attuale era late-ART) sia a livello di singolo paziente, la salute metabolica affronta i cambiamenti antropometrici e metabolici che accompagnano i pazienti nei punti di svolta fondamentali della malattia, tra cui l’inizio dell’ART, il passaggio all’ART e l’invecchiamento con l’HIV. L’obiettivo clinico di raggiungere una buona salute metabolica promette di migliorare il benessere e la qualità della vita delle PWH.
Se leggiamo PASO DOBLE nel quadro della salute metabolica, il punto è: TAF offre un vantaggio metabolico nelle persone con HIV? No, a livello farmacologico TAF associato a INSTI non migliora la salute metabolica. Tuttavia, il quadro della salute metabolica dovrebbe essere inserito in una prospettiva clinica e non farmacologica. Vale a dire: ci sono persone con HIV che traggono beneficio da TAF oltre all’INSTI? Sì, almeno come condizione di prudenza nelle persone che iniziano la terapia antiretrovirale in cui la singola risposta viro-immunologica è ancora sconosciuta o nel caso in cui è raccomandata una barriera genetica più elevata.
Ma c’è ancora un elefante nella stanza. Crediamo davvero che la salute metabolica dipenda solo dai farmaci antiretrovirali? La personalizzazione della terapia antiretrovirale ora implica l’uso contemporaneo di farmaci metabolicamente attivi, in particolare le statine, che potrebbero essere prese in considerazione nella stragrande maggioranza delle persone con HIV (8). Inoltre, nel sottoinsieme di persone con HIV ad alto rischio metabolico e obesità, non dovrebbero esserci ostacoli per quanto riguarda l’accesso alla nuova generazione di farmaci tra cui l’acido bependoico, il PCSK9, gli agonisti del GLP1 e gli inibitori del SGLT2, che hanno tutti dimostrato di fornire un beneficio multiorgano e di ridurre gli eventi cardio-metabolici (9-12).
In un approccio incentrato sul paziente, la prescrizione di ART dovrebbe sempre essere nel contesto di una valutazione metabolica al fine di educare e di conseguenza responsabilizzare le persone con HIV verso pratiche di vita sane. Il controllo dell’aumento di peso è un obiettivo condiviso sia per i medici che per i pazienti ed è un’opportunità per tracciare una tabella di marcia per ridurre il divario di una minore aspettativa di vita senza comorbilità e aumentare la qualità della vita per tutte le persone con HIV.
- Freitas P, Carvalho D, Santos AC, et al. Prevalence of obesity and its relationship to clinical lipodystrophy in HIV-infected adults on anti-retroviral therapy. J Endocrinol Invest 2012; 35:964–970.
- Nduka CU, Uthman OA, Kimani PK, Stranges S. Body Fat Changes in People Living with HIV on Antiretroviral Therapy. AIDS Rev 2016; 18:198–211.
- Venter WDF, Moorhouse M, Sokhela S, et al. Dolutegravir plus Two Different Prodrugs of Tenofovir to Treat HIV. N Engl J Med 2019; :NEJMoa1902824. Available at: http://www.nejm.org/doi/10.1056/NEJMoa1902824.
- Achhra AC, Mocroft A, Reiss P, et al. Short-term weight gain after antiretroviral therapy initiation and subsequent risk of cardiovascular disease and diabetes: The D: A: D study. HIV Med 2016; 17:255–268.
- Martinez E. Non-inferior efficacy and less weight gain when switching to DTG/3TC than when switching to BIC/FTC/TAF in virologically suppressed people with HIV (PWH): the PASODOBLE (GeSIDA 11720) randomised clinical trial. Abstract: OAB3606LB; presented at IAS 2024. Available at: https://programme.aids2024.org/Abstract/Abstract/?abstractid=12253. Accessed 3 October 2024.
- Milic J, Renzetti S, Ferrari D, et al. Relationship between weight gain and insulin resistance in people living with HIV switching to INSTI-based regimens. AIDS 2022;
- Mussini C, Guaraldi G. The best place for doravirine. lancet HIV 2024; 11:e64–e65.
- Grinspoon KS, Fitch VK, Zanni VM, et al. Pitavastatin to Prevent Cardiovascular Disease in HIV Infection. N Engl J Med 2023; 389:687–699. Available at: https://doi.org/10.1056/NEJMoa2304146.
- Nissen SE, Lincoff AM, Brennan D, et al. Bempedoic Acid and Cardiovascular Outcomes in Statin-Intolerant Patients. N Engl J Med 2023; 388:1353–1364.
- Sabatine MS, Giugliano RP, Keech AC, et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med 2017; 376:1713–1722.
- Lincoff AM, Brown-Frandsen K, Colhoun HM, et al. Semaglutide and Cardiovascular Outcomes in Obesity without Diabetes. N Engl J Med 2023; :NEJMoa2307563.
- McGuire DK, Shih WJ, Cosentino F, et al. Association of SGLT2 Inhibitors With Cardiovascular and Kidney Outcomes in Patients With Type 2 Diabetes: A Meta-analysis. JAMA Cardiol 2021; 6:148–158.







