Oggi, in tema di HIV, si mira al getting to zero: gli obiettivi del piano UNAIDS puntano a fare scendere le nuove infezioni da HIV da 1,3 milioni (diagnosticate nel 2023) fino a 370.000 nel 2025 e, addirittura, a zero nel 2030. Per raggiungere questi obiettivi, sono necessari strumenti potenti per fermare l’epidemia.
La profilassi pre-esposizione all'HIV (PrEP) con farmaci antiretrovirali è uno degli approcci più efficaci per prevenire l'HIV nelle popolazioni ad alto rischio. Attualmente, si stima che nel mondo circa 3,5 milioni di persone assumano regolarmente la PrEP e che più di 8 milioni l'abbiano iniziata almeno una volta. L’obiettivo UNAIDS è di raggiungere nel 2025 un numero di utilizzatori PrEP pari a circa 21 milioni a livello globale.
In Europa, il target dovrebbe essere di circa 500.000 persone in PrEP. Tuttavia, l’European Centre for Disease Prevention and Control (ECDC) stima che molto meno del 50% delle persone ad altissimo rischio di acquisizione dell'HIV e appena il 5% di quelle a rischio moderato accedono alla PrEP. I Paesi che hanno maggiormente implementato la PrEP al 2023 sono nell’ordine Francia (52.802 PrEP users), Germania (40.000 PrEP users), Spagna (23.600 PrEP users) e Italia (11.665 PrEP users).
Dallo studio ItaPrEP alla coorte PrIDE
L’inizio della PrEP in Italia risale al 2017, anno in cui ne veniva autorizzato l’utilizzo ma non la rimborsabilità, che è invece arrivata solo nel maggio 2023.
Nell’epoca in cui la PrEP non era rimborsabile, solo 8 centri nelle tre principali città eroganti PrEP (Roma, Milano e Bologna) erano riusciti a raccogliere dati attraverso il network dello studio ItaPrEP, promosso dalla Società Italiana di malattie infettive e tropicali (SIMIT). Tale studio ha fornito dati preziosi sui partecipanti, contribuendo a delineare il profilo degli utilizzatori PrEP tipo in Italia: dei 1758 partecipanti con dati completi, il 98.5% sono uomini gay italiani, con un’età mediana di circa 36 anni, la maggior parte con un buon livello di istruzione e per lo più con un lavoro stabile. Donne cis- e transgender rappresentano insieme meno del 2%, solo il 3% sono lavoratori del sesso e neanche il 5% ha meno di 25 anni. La fotografia che ci restituisce lo studio è dunque quella del consumo di PrEP da parte di una élite che lascia largamente fuori diverse altre popolazioni ad alto rischio. Il tasso di sieroconversioni è di 0.18 su 100 anni-persona di follow-up, suggerendo che, nonostante la mancanza di rimborsabilità, la PrEP in Italia è fattibile ed efficace.
Lo studio ha inoltre descritto due aspetti fondamentali della popolazione in PrEP: il tasso di aderenza alla PrEP e quello di interruzione (discontinuation) dal programma. Dopo il primo anno di inizio di PrEP, la probabilità di assumerla con scarsa aderenza è già del 40%; tale percentuale sale quasi al 60% dopo due anni e al 75.4% a 4 anni. Simile la situazione per la discontinuation: dopo il primo anno, quasi il 25% degli utilizzatori interrompe il programma di visite per assumere la PrEP e dopo 4 anni circa la metà degli utilizzatori risulta perso al follow-up. I predittori di tali comportamenti sono risultati l’utilizzo di chemsex, il basso livello di istruzione, la giovane età e la barriera dei costi su farmaci e monitoraggio.
Con l’arrivo della rimborsabilità di TDF/FTC, la barriera del costo del farmaco è stata abbattuta: l’aumento degli utilizzatori PrEP in tutti i centri è stato esponenziale e si è reso estremamente necessario uno strumento collettore dei dati della PrEP in Italia. Con tale intento è nata la coorte PrIDE (Prevention ICONA Dedicated Ensemble), che si propone di mettere insieme i centri, ospedalieri e non, che in Italia erogano PrEP.
Grazie al network della Fondazione ICONA, sono stati inizialmente raggiunti 57 centri a cui è stata inviata una survey, sia nel 2023 che nel 2024, che indagasse il volume di utilizzatori PrEP in ogni centro. Dal 2023 al 2024 si è registrato un incremento del numero di utilizzatori PrEP in tutte le regioni italiane, passando da un totale di circa 11.325 a più di 16.220, con un incremento percentuale del 43.22% a livello nazionale. Alcune regioni hanno registrato aumenti particolarmente significativi, come la Sardegna (+71.43%), il Friuli (+65.43%) e l'Emilia Romagna (+54.67%). Ancora però il numero assoluto di utilizzatori PrEP varia enormemente da regione a regione, mostrando una distribuzione poco capillare: Lombardia, Lazio ed Emilia Romagna si confermano le tre regioni con più utilizzatori PrEP, circa il 76% del totale in Italia (Figura 1).

Al 31 gennaio 2025, ancora non tutti i centri che hanno partecipato alla survey hanno completato le procedure burocratiche per l’inizio dell’arruolamento nella coorte PrIDE: sono attivi al momento solo 7 dei 57 centri previsti, che hanno arruolato ad oggi un totale di 782 utilizzatori. Una semplice analisi descrittiva dei primi arruolati ci dice che la maggior parte degli utilizzatori PrIDE proviene dall'Italia (676), seguiti da altri paesi (105), Sud America (45), Asia (21), Nord America (6), Africa (7) ed Europa (26). La popolazione PrIDE è composta principalmente da individui di sesso maschile alla nascita (98.3%) e cisgender (96.91%). La maggior parte ha un orientamento omosessuale (89.27%) e una formazione universitaria (64.58%). Tale quadro ricalca sostanzialmente quello già visto nello studio ItaPrEP. La riflessione è dunque quella di trovare strategie di ampliamento dell’accesso alla PrEP, di coinvolgimento di centri non clinici che abbiano contatto sul territorio, e di offerta di diverse opzioni di prevenzione farmacologica. Se fino a pochi mesi fa quest’ultima strategia sembrava impossibile da applicare, da dicembre a oggi, tre centri facenti parte del network di PrIDE hanno finalmente iniziato l’erogazione della nuova PrEP per via iniettabile.
Gli utilizzatori PrEP in cabotegravir
L’utilizzo per via intramuscolare di cabotegravir è stato autorizzato per l’immissione in commercio per la PrEP da EMA nel 2023, e classificato da AIFA come farmaco di classe C(nn) nel marzo 2024. Nelle more dell’approvazione della rimborsabilità da parte della nostra agenzia regolatoria, alcuni centri si sono adoperati per acquistare cabotegravir ed iniziarne la somministrazione in un programma pilota. In tal senso, al mese di gennaio 2025, sono stati somministrati nei centri Istituto Spallanzani di Roma, Ospedale Sacco e Istituto San Raffaele di Milano, circa 200 fiale di cabotegravir ad altrettanti utilizzatori PrEP.
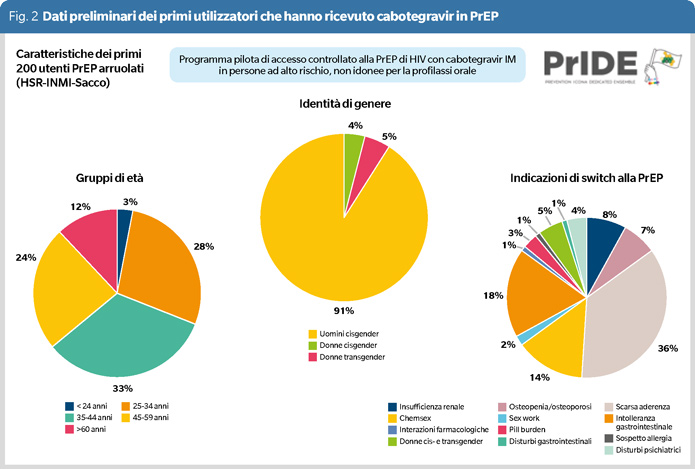
Anche tra questi utilizzatori della PrEP long acting, la maggior parte sono uomini cisgender, il 4% donne cisgender e il 5% donne transgender. La fascia di età più rappresentata è quella tra i 35 e i 44 anni (33%), seguita da quella tra i 25 e i 34 (28%) e poi tra i 45 e i 59 anni (24%). Il 12% aveva più di 60 anni, mentre solo il 3% meno di 24 anni (Figura 2).
Tale fotografia dei primi utilizzatori PrEP in cabotegravir ricalca da un lato il bacino di utenza afferente ai centri che erogano PrEP, come appunto già visto nelle precedenti coorti, ma anche il fatto che i diversi centri hanno utilizzato un criterio di erogazione orientato a dare priorità per l’accesso a cabotegravir a coloro che avevano problemi con la PrEP orale o che presentavano fattori di rischio per averne. In particolare, la scarsa aderenza alla PrEP orale ha rappresentato la principale ragione di prescrizione di cabotegravir (nel 36% degli utilizzatori) così come l’utilizzo di chemsex, fattore di rischio per la scarsa aderenza (nel 14%).
A seguire le altre ragioni di scelta della PrEP long acting erano la scarsa tollerabilità gastrointestinale della PrEP orale (18%), la tossicità renale (8%) o ossea (7%) e poi ancora, in percentuali poco rappresentative, patologie psichiatriche, altre comorbidità con elevato pill burden, essere donna cis- o transgender (Figura 2).
Tale prioritizzazione è stata adottata naturalmente dai centri visto il numero ridotto dei trattamenti a disposizione e le ancora poco sicure tempistiche dell’arrivo della rimborsabilità del farmaco sul mercato. Questa prima esperienza apre però le porte del futuro tra nuove soluzioni e nuove sfide. Se da un lato la PrEP iniettabile fa iniziare l’era della possibilità di multiple opzioni di scelta per la PrEP e di cambiare a soluzioni più confortevoli senza interrompere la protezione, dall’altro la modalità di somministrazione iniettabile pone sfide organizzative da risolvere e l’apertura alla demedicalizzazione dell’erogazione della PrEP nonché l’importanza dei centri community-based. La prossima survey 2025 di PrIDE ci aiuterà sicuramente a cogliere i nuovi cambiamenti.
- The urgency of now: AIDS at a crossroads. Joint United Nations Programme on HIV/AIDS, https://www.unaids.org/sites/default/files/media_asset/2024-unaids-global-aids-update_en.pdf.
- A map-based tool to explore trends in PrEP use globally as countries introduce and scale up PrEP programs., https://data.prepwatch.org/ (accessed 25 January 2025).
- Baeten JM, Donnell D, Ndase P, et al. Antiretroviral Prophylaxis for HIV Prevention in Heterosexual Men and Women. N Engl J Med 2012;367:399-410.
- Grant RM, Lama JR, Anderson PL, et al. Pre-exposure Chemoprophylaxis for HIV Prevention in Men Who Have Sex with Men. N Engl J Med 2010;363:2587-2599.
- McCormack S, Dunn DT, Desai M, et al. Pre-exposure prophylaxis to prevent the acquisition of HIV-1 infection (PROUD): effectiveness results from the pilot phase of a pragmatic open-label randomised trial. Lancet 2016;387:53-60.
- Molina J-M, Capitant C, Spire B, et al. On-Demand Pre-exposure Prophylaxis in Men at High Risk for HIV-1 Infection. N Engl J Med 2015; 373: 2237-2246.
- Cambiano V, Miners A, Lampe FC, et al. The effect of combination prevention strategies on HIV incidence among gay and bisexual men who have sex with men in the UK: a model-based analysis. Lancet HIV 2023;10:e713-e722.
- Landovitz RJ, Hanscom BS, Clement ME, et al. Efficacy and safety of long-acting cabotegravir compared with daily oral tenofovir disoproxil fumarate plus emtricitabine to prevent HIV infection in cisgender men and transgender women who have sex with men 1 year after study unblinding: a secondary analysis of the phase 2b and 3 HPTN 083 randomised controlled trial. Lancet HIV. 2023;10(12):e767-e778.
- Delany-Moretlwe S, Hughes JP, Bock P, et al. Cabotegravir for the prevention of HIV-1 in women: results from HPTN 084, a phase 3, randomised clinical trial [published correction appears in Lancet. 2022 May 7;399(10337):1778.] Lancet. 2022;399(10337):1779-1789.
- Mazzotta V, Calzavara D, Tavelli A, et al. HIV pre-exposure prophylaxis (PrEP) efficacy, adherence and persistence in an Italian multicentric access program (Sep2017-Nov2023):ItaPrEP study. OA1006 HIVR4P 2024 Abstract book, JIAS.







