La sindrome infiammatoria da immunoricostituzione (IRIS) è la risposta eccessiva del sistema immunitario verso vari patogeni, conseguente al suo recupero funzionale dopo immunosoppressione. Sebbene classicamente associata all’HIV, l’IRIS può verificarsi in immunodepressi per altre cause (malattie ematologiche, trapianti d’organo, terapie biologiche). Quando associata all’HIV, l’IRIS è correlata all’inizio della terapia antiretrovirale (ART). In altri casi, emerge col ridursi dell’immunosoppressione farmacologica o per una massiva presentazione antigenica, come nella tubercolosi (TB) disseminata in HIV-negativi.
I segni e sintomi derivano dal rapido ripristino della risposta immunitaria al ridursi dell’immunosoppressione. Fattori di rischio includono bassa conta di CD4+, alta carica virale, e l’entità della patologia sottostante (1,2), ma non esistono cut-off definiti.
L’incidenza è varia e difficilmente stimabile, presentandosi più frequentemente con sintomatologia lieve. Alcuni studi stimano un’incidenza del 16% per IRIS da malattia tubercolare (mortalità ~3%) e il 19.5% per IRIS da meningite criptococcica (mortalità ~21%), con picco di rischio fino al 28% per una conta di <50 CD4+/mm³, contro il 2% in quelli con conte superiori (3).
 Le tempistiche di presentazione sono molto variabili, dipendendo dal grado di immunodepressione, dalla quantità di malattia e dalla capacità di ripresa del sistema immunitario. Spesso si presenta tra 1 e 8 settimane (mediana 48 giorni) (4). In particolare, secondo alcuni studi l’IRIS si manifesta medianamente dopo 4 settimane dall’inizio dell’ART se associata a micobatteri (e nei primi 2 mesi di terapia antitubercolare) e dopo circa 9 settimane se associata a meningite criptococcica (5,6).
Le tempistiche di presentazione sono molto variabili, dipendendo dal grado di immunodepressione, dalla quantità di malattia e dalla capacità di ripresa del sistema immunitario. Spesso si presenta tra 1 e 8 settimane (mediana 48 giorni) (4). In particolare, secondo alcuni studi l’IRIS si manifesta medianamente dopo 4 settimane dall’inizio dell’ART se associata a micobatteri (e nei primi 2 mesi di terapia antitubercolare) e dopo circa 9 settimane se associata a meningite criptococcica (5,6).
Le presentazioni cliniche includono:
- paradoxical IRIS: peggioramento delle localizzazioni preesistenti di una patologia nota dopo un iniziale miglioramento
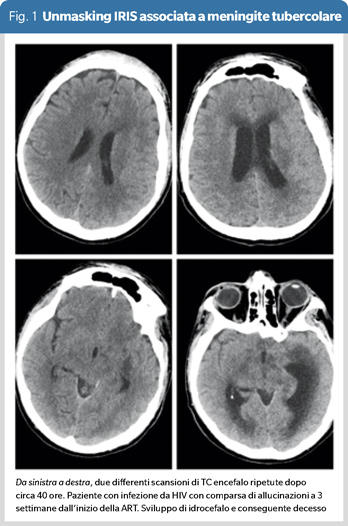
- unmasking IRIS: la reazione infiammatoria stessa “svela” un’infezione sottostante (Figura 1).
Il sintomo più comune, spesso unico, è la febbre, presente in almeno i tre quarti dei casi. Può presentarsi come febbricola o febbre elevata ma, per quanto prostrante, non è necessariamente indice di gravità. Gli altri sintomi sono più spesso legati alla patologia sottostante. Manifestazioni severe con interessamento del sistema nervoso centrale (SNC) sono meno comuni, ma potenzialmente letali.
IRIS e patogeni specifici
Micobatteri. Sintomi frequenti sono febbre, linfoadenopatie e peggioramento respiratorio (nel caso di micobatteriosi polmonare). In caso di malattia disseminata, i sintomi rispecchiano il coinvolgimento sistemico e, oltre ai sintomi citati, è possibile la comparsa di rallentamento ideomotorio, insufficienza renale o midollare e ipercalcemia, fino al decesso. La TB extrapolmonare o disseminata comporta un rischio significativamente maggiore di IRIS, probabilmente per l’elevato carico bacillare.
In assenza di infezione da HIV, l’IRIS può indicare ripresa immunitaria dopo la transitoria immunosoppressione causata dal micobatterio stesso o la massiva esposizione di antigeni micobatterici. Questa risposta non rappresenta necessariamente un indicatore di gravità. Pertanto, in assenza di compromissione dei parametri vitali o di segni gravi di danno d’organo, spesso non è richiesta una terapia specifica oltre a quella sintomatica. La sintomatologia e gli indici infiammatori tendono a normalizzarsi con il trattamento della TB.
Cryptococcus neoformans. Nella quasi totalità dei casi, l’IRIS legata a criptococcosi si presenta con peggioramento o comparsa di sintomatologia riferibile a meningite. I pazienti più predisposti a sviluppare IRIS dopo l’inizio della ART presentano: livelli di antigene criptococcico nel siero superiori di almeno 4 volte rispetto agli altri prima dell’avvio della ART, numero di leucociti nel liquor ≤25/mm³, protidorrachia <50 mg/dL e un elevato carico antigenico. Non esistono test o criteri diagnostici specifici per la diagnosi di IRIS, pertanto una valutazione clinica accurata è essenziale per guidare il trattamento, riservato solo ai casi gravi. La diagnosi di IRIS dovrebbe essere presa in considerazione in un paziente con:
- bassa conta di linfociti CD4+
- alta carica virale con importante risposta virologica
- manifestazioni cliniche compatibili con una condizione infiammatoria
- associazione temporale compatibile tra l’inizio della ART e sintomatologia.
Terapia
Per il trattamento dell’IRIS vanno considerati: la terapia dell’infezione sottostante, la ART e l’utilizzo di terapie aggiuntive.
L’infezione opportunistica deve essere trattata il prima possibile e in caso di peggioramento paradosso, la terapia antimicrobica mirata deve essere continuata, così come la ART se già iniziata. Questo approccio è tratto da studi che dimostrano che ritardare o interrompere la ART aumenta il rischio di sviluppare ulteriori complicanze associate all’immunosoppressione.
 In pazienti con HIV e TB polmonare con CD4+ <50/mm3, la ART dovrebbe essere iniziata entro 2 settimane dall’inizio della terapia antitubercolare per ridurre il rischio di sviluppare una patologia AIDS-definente e di morte. In pazienti con HIV e TB polmonare con CD4+ >50 cellule/mm3, la ART dovrebbe essere iniziata entro 8 settimane. In assenza di un quadro clinico grave, un inizio posticipato della ART (entro 8 settimane) è associato ad una riduzione del rischio di IRIS (7). In persone con TB del SNC invece, la ART dovrebbe essere posticipata oltre le 8 settimane dall’inizio della terapia antitubercolare, indipendentemente dal numero di CD4+. Essendo l’IRIS una condizione mediata dal sistema immunitario, i farmaci che modulano le risposte dell’ospite possono avere un ruolo terapeutico.
In pazienti con HIV e TB polmonare con CD4+ <50/mm3, la ART dovrebbe essere iniziata entro 2 settimane dall’inizio della terapia antitubercolare per ridurre il rischio di sviluppare una patologia AIDS-definente e di morte. In pazienti con HIV e TB polmonare con CD4+ >50 cellule/mm3, la ART dovrebbe essere iniziata entro 8 settimane. In assenza di un quadro clinico grave, un inizio posticipato della ART (entro 8 settimane) è associato ad una riduzione del rischio di IRIS (7). In persone con TB del SNC invece, la ART dovrebbe essere posticipata oltre le 8 settimane dall’inizio della terapia antitubercolare, indipendentemente dal numero di CD4+. Essendo l’IRIS una condizione mediata dal sistema immunitario, i farmaci che modulano le risposte dell’ospite possono avere un ruolo terapeutico.
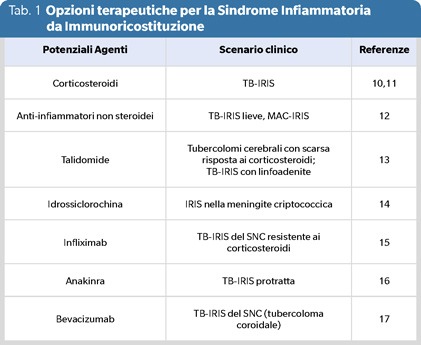
Le raccomandazioni si basano principalmente su serie di casi e opinioni di esperti con pochi studi controllati (8,9) (Tabella 1).
In uno studio randomizzato controllato in pazienti affetti da IRIS-TB, il prednisone è stato somministrato per 2 settimane alla dose di 1.5 mg/kg al giorno e per 2 settimane alla dose di 0.75 mg/kg al giorno (10).
I pazienti che hanno ricevuto prednisone rispetto al placebo hanno mostrato un numero mediano di giorni di ospedalizzazione inferiore e miglioramenti significativi dei sintomi. Un altro studio randomizzato controllato (11) ha utilizzato il prednisone in profilassi evidenziando un miglioramento della funzionalità polmonare a 4 settimane, in assenza di benefici a lungo termine. Complessivamente in questi studi il prednisone è stato ben tollerato.
I FANS possono alleviare i sintomi dell’infiammazione sistemica in pazienti con manifestazioni minori di IRIS da TB e Mycobacterium avium complex, ma non sono stati mai valutati in studi randomizzati controllati (12).
La talidomide è conosciuta per le sue caratteristiche antiangiogeniche e immunomodulatorie (principalmente riducendo il TNF-α). È stata impiegata con miglioramento clinico in un paziente con IRIS e linfoadenite tubercolare e con miglioramento clinico e radiografico in pazienti senza infezione da HIV con tubercolomi intracranici con scarsa risposta ai corticosteroidi (13).
L’idrossiclorochina esercita i suoi effetti antinfiammatori/immunomodulatori interferendo con l’elaborazione e la presentazione dell’antigene attraverso le molecole del complesso maggiore di istocompatibilità di classe II. Riduce inoltre la produzione di citochine infiammatorie come IL-1, IL-6 e TNF-α. È stata utilizzata in combinazione con il metilprednisolone e l’interruzione della ART per trattare con successo un caso di meningite criptococcica-IRIS (14).
Due case report hanno riportato l’utilizzo di infliximab (TNF-α) in pazienti con IRIS-TB del SNC resistente ai corticosteroidi (15). In un caso sono state somministrate tre dosi di infliximab a intervalli mensili con buona risposta clinica e radiologica. Altri due case report hanno evidenziato l’utilizzo di adalimumab con beneficio in pazienti con IRIS-TB del SNC refrattaria.
Anakinra è un antagonista del recettore dell’IL-1. In un case report anakinra è stato utilizzato con successo in due pazienti con reazioni paradosse protratte da IRIS-TB per controllare l’infiammazione e ridurre la terapia steroidea fino alla sospensione (16).
In un case report bevacizumab (inibitore VEGF) è stato utilizzato a livello intravitreale in una IRIS-TB del SNC (tubercoloma coroidale) con risoluzione del distacco retinico sieroso refrettario alle comuni terapie (17).
- Grant PM, Komarow L, Andersen J, et al. Risk factor analyses for immune reconstitution inflammatory syndrome in a randomized study of early vs. deferred ART during an opportunistic infection. PLoS One. 2010;5(7):e11416.
- Breton G, Duval X, Estellat C, et al. Determinants of immune reconstitution inflammatory syndrome in HIV type 1-infected patients with tuberculosis after initiation of antiretroviral therapy. Clin Infect Dis. 2004;39(11):1709-1712.
- Müller M, Wandel S, Colebunders R, et al. Immune reconstitution inflammatory syndrome in patients starting antiretroviral therapy for HIV infection: a systematic review and meta-analysis. Lancet Infect Dis. 2010;10(4):251-261.
- Murdoch DM, Venter WD, Feldman C, et al. Incidence and risk factors for the immune reconstitution inflammatory syndrome in HIV patients in South Africa: a prospective study. AIDS. 2008;22(5):601-610.
- Lawn SD, Bekker LG, Miller RF. Immune reconstitution disease associated with mycobacterial infections in HIV-infected individuals receiving antiretrovirals. Lancet Infect Dis. 2005;5(6):361-373.
- Boulware DR, Meya DB, Bergemann TL, et al. Clinical features and serum biomarkers in HIV immune reconstitution inflammatory syndrome after cryptococcal meningitis: a prospective cohort study. PLoS Med. 2010;7(12):e1000384.
- World Health Organization. Guidelines for treatment of drug-susceptible tuberculosis and patient care, 2017 update.
- Vinhaes CL, Araujo-Pereira M, Tibúrcio R, et al. Systemic Inflammation Associated with Immune Reconstitution Inflammatory Syndrome in Persons Living with HIV. Life (Basel). 2021;11(1):65.
- Quinn CM, Poplin V, Kasibante J, et al. Tuberculosis IRIS: Pathogenesis, Presentation, and Management across the Spectrum of Disease. Life (Basel). 2020;10(11):262.
- Meintjes G, Wilkinson RJ, Morroni C, et al. Randomized placebo-controlled trial of prednisone for paradoxical tuberculosis-associated immune reconstitution inflammatory syndrome. AIDS 2010;24:2381-90.
- Stek C, Allwood B, Du Bruyn E, et al. The effect of HIV-associated tuberculosis, tuberculosis-IRIS and prednisone on lung function. Eur Respir J.2020;55(3):1901692.
- Marais S, Wilkinson RJ, Pepper DJ, Meintjes G. Management of patients with the immune reconstitution inflammatory syndrome. Curr HIV/AIDS Rep. 2009;6(3):162-71.
- Schoeman JF, Fieggen G, Seller N, et al. Intractable intracranial tuberculous infection responsive to thalidomide: report of four cases. J Child Neurol. 2006;21(4):301-8.
- Boelaert JR, Goddeeris KH, Vanopdenbosch LJ, Casselman JW. Relapsing meningitis caused by persistent cryptococcal antigens and immune reconstitution after the initiation of highly active antiretroviral therapy. AIDS. 2004;18(8):1223-4.
- Blackmore TK, Manning L, Taylor WJ, Wallis RS. Therapeutic use of infliximab in tuberculosis to control severe paradoxical reaction of the brain and lymph nodes. Clin Infect Dis. 2008;47(10):e83-5.
- Keeley AJ, Parkash V, Tunbridge A, et al. Anakinra in the treatment of protracted paradoxical inflammatory reactions in HIV-associated tuberculosis in the United Kingdom: a report of two cases. Int J STD AIDS. 2020;31(8):808-812.
- Jain S, Bajgai P, Tigari B, et al. Bevacizumab for paradoxical worsening treatment adjunct in HIV patient with choroidal tuberculoma. J Ophthalmic Inflamm Infect. 2016;6(1):42.







