|
| |
| Valutazione e gestione del paziente con HIV e comorbidità renale:
focus sui nuovi regimi terapeutici |
|
|
| |
Il primo di questi farmaci è rilpivirina, inibitore non nucleosidico della trascrittasi inversa, che ha un'alta capacità di legame proteico ed è escreta solo in minima parte dal rene.
In due ampi trial clinici è stato registrato un incremento della creatinina sierica (SCr) di circa 0.1 mg/dl in pazienti che presentano normale funzione renale.
Questo incremento, stabile nel tempo e non associato ad altri segni laboratoristici di danno renale, a sua volta influenzava la stima del GFR basata sulla creatinina (eGFRcreat) (figura 1).
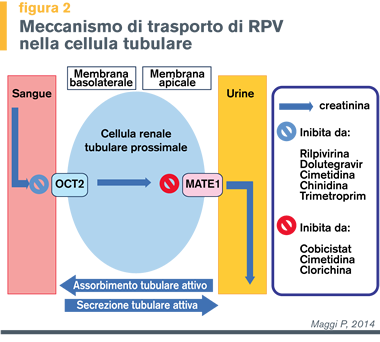
Rilpivirina agisce come inibitore del renal organic cationic transporter (OCT2), recettore presente sul versante basolaterale del tubulo renale prossimale (figura 2), con un meccanismo che mima quello di cimetidina, chinidina o trimethoprim; tutti questi farmaci diminuiscono la secrezione di creatinina a livello del tubulo renale prossimale.
|
 |
|
| |
 |
Il GFR stimato con formule basate sulla cistatina C sierica (eGFRcys) non mostra riduzioni in corso di trattamento con rilpivirina.
Tuttavia è opportuna una certa prudenza nell’usare questa formula a causa di possibili variazioni nella secrezione di cistatina C, in relazione allo stato virologico del paziente (1). |
|
| |
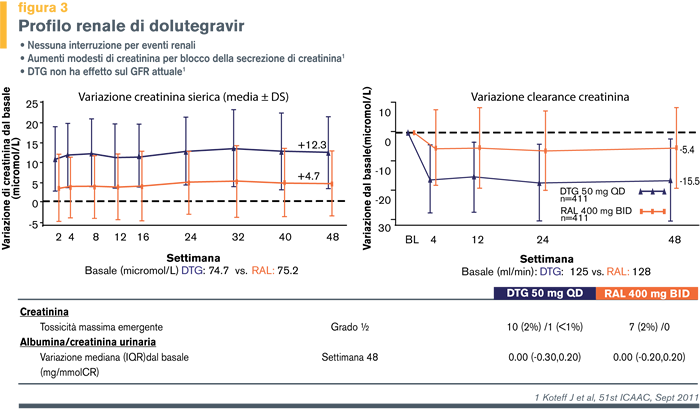
| Dolutegravir è un nuovo inibitore dell’integrasi metabolizzato dall'UGT1A1 epatico e dal CYP3A, sebbene con un ruolo minore di quest'ultimo. L'eliminazione renale di dolutegravir immodificato è <1%. In uno studio comparativo vs raltegravir (SPRING), è emerso un modico incremento di creatininemia nel braccio dolutegravir [2] (figura 3). |
| |
 |
| |
Anche in questo caso si trattava di un incremento lieve e non progressivo, nel range di 0.1 – 0.15 mg/dL, senza effetti sul reale filtrato glomerulare (a-GFR), misurato con la clearance dello iohexolo [3,4] (figura 4).
Anche in questo caso, i dati clinici e in vitro sono coerenti con un’inibizione di OCT2.
L’inibizione farmacologica di OCT2 blocca la secrezione tubulare di creatinina (figura 2). |
 |
|
| |
 |
Cobicistat è un nuovo enhancer farmacocinetico, metabolizzato dal CYP3A, che non ha alcuna proprietà antiretrovirale di per sé.
Cobicistat provoca un incremento della SCr e un conseguente decremento dell'eGFR basato sulla stima della creatinina. Precedenti studi hanno dimostrato che cobicistat è un potente inibitore di MATE1 (Human Multidrug and Toxic Extrusion 1), recettore presente a livello del polo apicale della cellula tubulare renale, ed è responsabile dell’efflusso della creatinina dalle cellule tubulari [5] (figura 1).
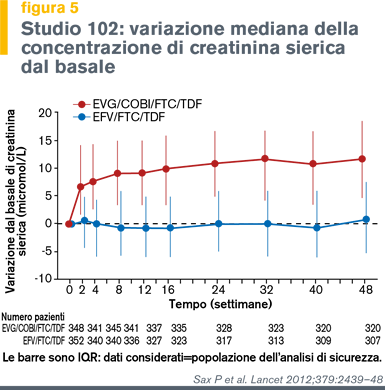
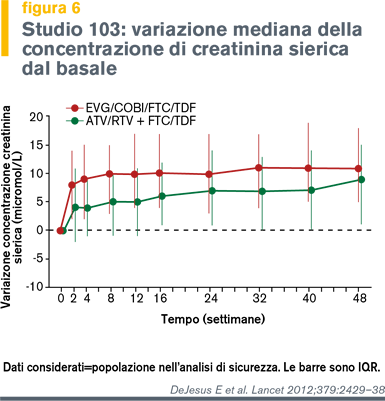
Di conseguenza, cobicistat inibisce la quota di secrezione tubulare di creatinina causando un lieve (< 10%) incremento della creatinina sierica, con conseguente riduzione dell'eGFRcreat senza altre evidenze di danno renale (figure 5 e 6). |
 |
Queste alterazioni laboratoristiche sono prontamente reversibili dopo sospensione del farmaco.
I fenomeni descritti possono dunque essere considerati un reset dell'eGFRcreat. Tuttavia i clinici dovranno monitorare attentamente la funzione renale al fine di identificare prontamente alterazioni suggestive di una vera alterazione. L’introduzione di questi nuovi farmaci richiederà pertanto l’utilizzo di parametri di disfunzione renale semplici e affidabili che esplorino sia la filtrazione glomerulare che il danno tubulare. Data l’interferenza di questi farmaci con la secrezione tubulare della creatinina, una metodica alternativa di stima del GFR sarebbe desiderabile, sebbene al momento non sia disponibile. |
|
| |
Infatti metodi di misurazione diretta di inulina, ioexolo o iotalamato plasma, se da un lato aiuterebbero a superare questo problema, dall’altro richiedono ripetuti prelievi, non sono facilmente disponibili e richiedono procedure analitiche complesse. Per altro, le formule dell'eGFR basate sulla cistatina C, pur avendo una buona performance nella popolazione libera [6], sono poco affidabili nei pazienti con HIV [7-10].
L’eGFR stimato con formule affidabili come il CKD-EPIcreat sè ancora raccomandato anche nei pazienti trattati con questi farmaci, pur considerando che regimi includenti rilpivirina, dolutegravir o cobicistat produrranno un’apparente riduzione dell'eGFRcreat che, in condizioni normali non dovrebbe eccedere il 25% rispetto al livello basale.
Una riduzione maggiore dell'eGFRcreat dovrà essere, quindi, valutata con attenzione perché potrebbe rappresentare il segno di una reale alterazione della funzione renale. Oltre alla valutazione del filtrato glomerulare, la funzione tubulare dovrebbe essere attentamente monitorata con test di screening semplici quali la proteinuria all’esame delle urine.
Una proteinuria patologica al test di screening, avendo un alto valore predittivo negativo, ma un basso positivo, andrebbe confermata con lo studio della proteinuria quantitativa su urine spot del mattino (proteinuria totale/creatinuria=PCR e albuminuria/creatinuria=ACR). Il rapporto tra ACR e PCR può discriminare tra una proteinuria glomerulare e tubulare [11].
Una disfunzione tubulare può essere sospettata in presenza di ipofosfatemia, iperfosfaturia di un’aumentata escrezione frazionale di acido urico. Una glicosuria normoglicemica è un segno avanzato di disfunzione tubulare.
Secondo le nuove Linee Guida Italiane 2013, pazienti in trattamento con cobicistat e dolutegravir andranno monitorati mensilmente per i primi tre mesi e, successivamente, ogni quattro mesi. Un calo dell'eGFRcreat maggiore del 25% o insorgenza de novo di segni di disfunzione tubulare necessiteranno di una valutazione nefrologica. Per i pazienti che ricevono rilpivirina invece non è necessario un monitoraggio specifico. |
| |
|
Bibliografia
- Cohen CJ, Molina JM, Cassetti I et al., Week 96 efficacy and safety of rilpivirine in treatment-naive, HIV-1 patients in two Phase III randomized trials. AIDS 2013, 27:939–950.
- Raffi F, Rachlis A, Stellbrink HJ et al. Once-daily dolutegravir versus raltegravir in antiretroviral-naive adults with HIV-1 infection: 48 week results from the randomised, double-blind, non-inferiority SPRING-2 study. Lancet. 2013;381:735-774.
- Koteff J, Borland J, Chen S et al. A phase 1 study to evaluate the effect of dolutegravir on renal function via measurement of iohexol and para-aminohippurate clearance in healthy subjects. Br J Clin Pharmacol 2012;75:990-996.
- Stellbrink HJ, Reynes J, Lazzarin A et al. Dolutegravir (DTG; S/GSK1349572) in Combination Therapy Exhibits Rapid and Sustained Antiviral Response in Antiretroviral‐Naïve Adults: 96‐Week Results from SPRING‐1 (ING112276) 19th CROI.8 Mar 2012. Abstract K-102.
- Meyer zu Schwabedissen HE, Verstuyft C, Kroemer HK et al. Human multidrug and toxin extrusion 1 (MATE1/SLC47A1) transporter: functional characterization, interaction with OCT2 (SLC22A2), and single nucleotide polymorphisms. Am J Physiol Renal Physiol. 2010;298(4):F997-F1005.
- Stevens LA, Coresh J, Schmid CH et al. Estimating GFR using serum cystatin C alone and in combination with serum creatinine: a pooled analysis of 3,418 individuals with CKD. Am J Kidney Dis. 2008;51:395-406.
- Jaroszewicz J, Wiercinska-Drapalo A, Lapinski TW et al. Does HAART improve renal function? An association between serum cystatin C concentration, HIV viral load and HAART duration. Antivir Ther. 2006;11:641-645.
- Longenecker CT, Scherzer R, Bacchetti P et al. HIV viremia and changes in kidney function. AIDS. 2009;23:1089-1096.
- Mauss S, Berger F, Kuschak D et al. Cystatin C as a marker of renal function is affected by HIV replication leading to an underestimation of kidney function in HIV patients. Antivir Ther. 2008;13:1091-1095.
- Odden MC, Scherzer R, Bacchetti P et al. Cystatin C level as a marker of kidney function in human immunodeficiency virus infection: the FRAM study. Arch Intern Med. 2007;167:2213-2219.
- Samarawickrama A, Cai M, Smith ER et al. Simultaneous measurement of urinary albumin and total protein may facilitate decision-making in HIV-infected patients with proteinuria. HIV Medicine 2012. 13:526-32.
|