Al basale, i pazienti nel braccio EVG/COBI/TDF/FTC presentavano una mediana di HIV RNA di 4.75 log10 copie/ml e una conta media di CD4 di 391 cellule/mmc. I pazienti in terapia con EFV/TDF/FTC avevano una mediana di HIV RNA di 4.70 log10 copie/ml e una conta media di CD4 di 382 cellule/mmc.
Il 34% dei pazienti in EVG/COBI/TDF/FTC e il 33% di quelli in EFV/TDF/FTC presentava livelli di viremia superiori a 100.000 copie/ml. Il 12% dei pazienti in EVG/COBI/TDF/FTC e il 14% dei pazienti in EFV/TDF/FTC avevano conte di CD4 ≤ 200 cellule/mmc.
A 48 settimane di terapia (5) EVG/COBI/TDF/FTC era risultato non inferiore a EFV/TDF/FTC (rispettivamente, l’88% vs 84.% dei pazienti avevano un HIV-RNA < 50 copie/ml, IC95% -1.6%-8.8%), il successo virologico si era mantenuto a 96 settimane (84% vs 82% , IC95% -2.9% - 8.3%) (12) ed è stato confermato alla settimana 144 di trattamento in modo analogo nei diversi sottogruppi di pazienti (stratificati per caratteristiche demografiche, livelli basali di viremia e di CD4) (Figure 5 e 6).
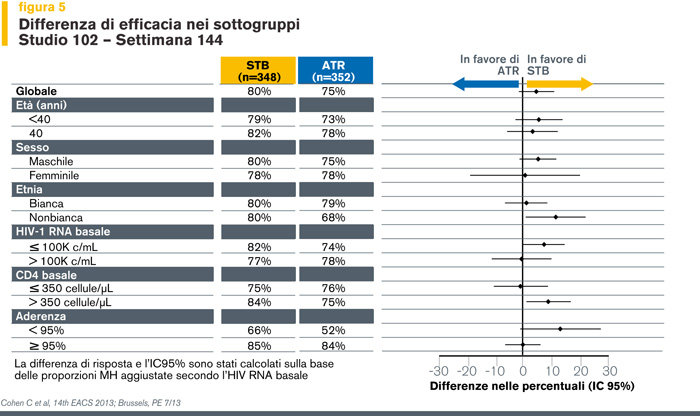
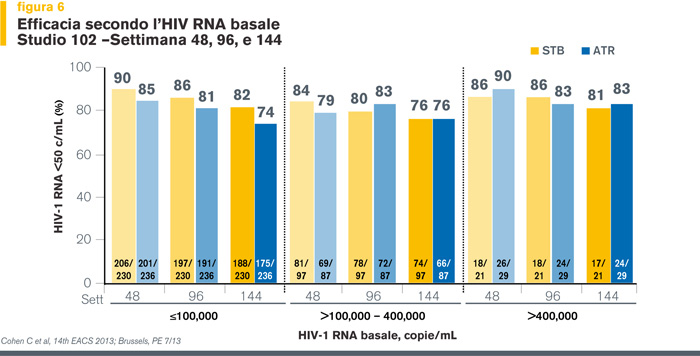
Di particolare importanza è il dato secondo cui l’efficacia clinica di EVG/COBI/TDF/FTC è confermata anche nei pazienti con alte viremie basali (≥ 100.000 copie/ml e >400.000 copie/ml).
A 48 settimane (5) gli aumenti medi di CD4 erano significativamente superiori nel gruppo EVG/COBI/TDF/FTC rispetto a EFV/TDF/FTC (+ 239 cellule/mmc vs + 206 cellule/mmc, p=0.009). Tra la settimana 48 e 96 settimane (12) le conte di CD4 hanno continuato ad aumentare in modo simile nei due gruppi (a 96 settimane rispettivamente + 295 cellule/mmc vs + 273 cellule/mmc, p=0.19).
L’efficacia immunologica del nuovo STR si è mantenuta a 144 settimane di follow up, gli aumenti medi di CD4 rispetto al valore basale erano pari a +321 cellule/mmc per i pazienti in EVG/COBI/TDF/FTC e a +300 cellule/mmc nei pazienti in EFV/TDF/FTC.
I tassi di fallimento virologico sono stati pari al 7% per EVG/COBI/TDF/FTC e al 10% per EFV/TDF/FTC sulla base dell’analisi snapshot (14, 15), che dimostra il mantenimento dell’efficacia e della sicurezza a lungo termine del nuovo STR (Figura 3).

Nel corso delle 144 settimane, il 6% dei pazienti che ricevevano il nuovo STR e l’8% di quelli in EFV/TDF/FTC hanno interrotto il trattamento a causa di eventi avversi. Gli eventi avversi (AE) che hanno comportato l’interruzione sono stati rispettivamente eventi renali (2.3%), depressione (0.3%) e facile stancabilità (0.3%), mentre tra i pazienti in terapia con EFV/TDF/FTC sono stati depressione (1.4%), rash e ipersensibilità al farmaco (1.4%), facile stancabilità (0.6%), sogni vigili (0.6%), insonnia (0.6%) e ansia (0.6%) (Figura 7).
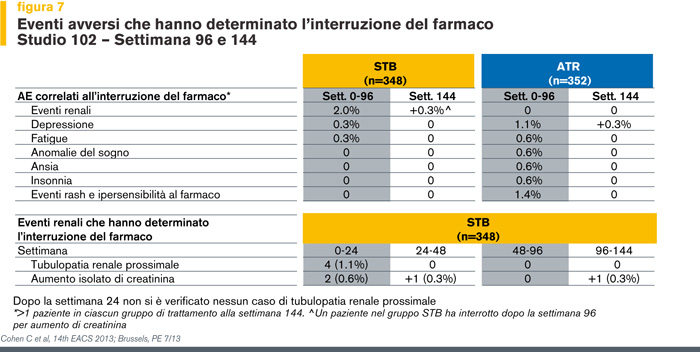
La frequenza di eventi avversi e di alterazioni di laboratorio di grado 3-4 è stata simile tra i regimi (Figura 8).
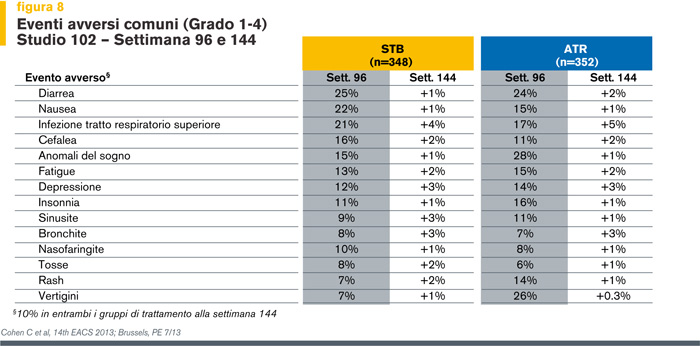
La variazione media dal basale di colesterolo totale e colesterolo LDL a 144 settimane è stata inferiore per EVG/COBI/TDF/FTC in confronto a EFV/TDF/FTC: rispettivamente, +14 mg/dl e +13 mg/dl per EVG/COBI/TDF/FTC e +22 mg/dl e +19 mg/dl per EFV/TDF/FTC (colesterolo totale, p=0.007; LDL p=0.007).
Le variazioni medie dal basale delle LDL e dei trigliceridi sono risultate simili in entrambi i gruppi, rispettivamente pari a +7 mg/dl e +9 mg/dl per il nuovo STR e a +9 mg/dl e +5 mg/dl per EFV/TDF/FTC (HDL p=0.021; trigliceridi p=0.72).
Gli aumenti medi a 144 settimane della creatinina sierica rispetto al valore basale sono stati 0.14 mg/dl per EVG/COBI/TDF/FTC e 0.01 mg/dl per EFV/TDF/FTC. Nel corso delle prime 24 settimane di terapia si sono verificati 4 casi (1.1%) di tubulopatia renale prossimale nei pazienti che ricevevano EVG/COBI/TDF/FTC (tutti i pazienti sono migliorati alla sospensione del farmaco (18)), e nessuno successivamente (Figura 7).
Tra la settimana 96 e 144 di terapia, un paziente in EVG/COBI/TDF/FTC ha interrotto il trattamento a causa di un rialzo isolato di creatinina, senza manifestazioni di tubulopatia renale prossimale, che è migliorato dopo l’interruzione del farmaco.
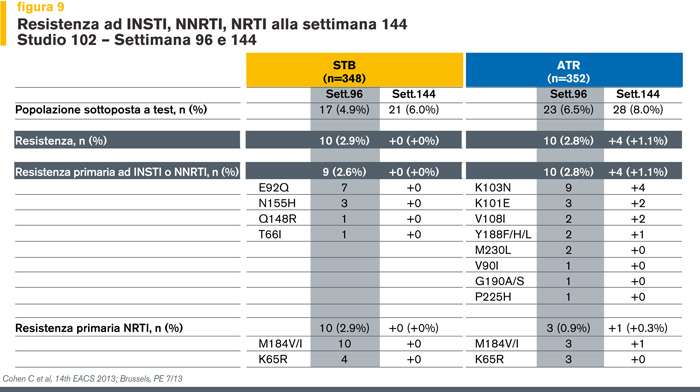
Mentre nei fallimenti virologici a 96 settimane si sono osservati 9 casi di mutazioni associate a resistenza per INSTI, non si sono osservati casi di sviluppo di resistenze nel braccio di pazienti EVG/COBI/TDF/FTC tra la settimana 96 e 144 di terapia (Figura 9).
|