|
| |
| HBV e farmacoresistenza |
| Farmacoresistenza e immunogenicità virale |
| |
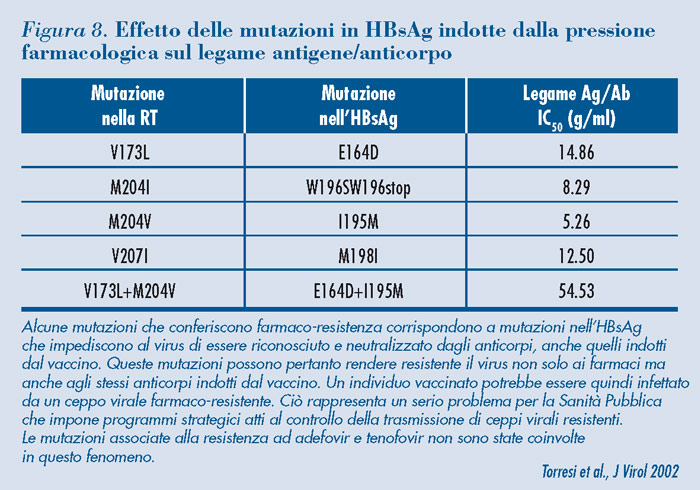
| La pressione esercitata dai farmaci è in grado di indurre mutazioni non solo nella trascrittasi inversa ma anche nell’HBsAg, ed in particolare, negli epitopi riconosciuti dagli anticorpi neutralizzanti. Questo fenomeno, che è stato descritto per le mutazioni chiave coinvolte nella resistenza alla lamivudina (ed in particolare per il pattern composto dalle mutazioni M204V, L180M e V173L) è in grado di rendere il virus resistente non solo ai farmaci nucleosidici (lamivudina, telbivudina, entecavir) ma anche agli anticorpi neutralizzanti, in alcuni casi anche quelli indotti dal vaccino (Figura 8). |
| |
 |
| |
| Fortunatamente questo fenomeno non coinvolge le mutazioni di resistenza agli analoghi nucleotidici, che danno origine a mutazioni nell’HBsAg che non compromettono il riconoscimento da parte degli anticorpi neutralizzanti. L’argomento è comunque di grande importanza in quanto suggerisce di limitare al minimo lo sviluppo di resistenze, date le molteplici conseguenze, anche immunologiche, che ciò comporta. L’uso di farmaci potenti e ad alta barriera genetica diventa quindi ancor più cogente nella pratica clinica, anche e soprattutto nei pazienti, che avendo deficit immunologici in atto, possono andare incontro oppure già abbiano una riattivazione virale. Ciò mette sostanzialmente in dubbio l’utilità/opportunità del trattamento con lamivudina nei pazienti immunosoppressi, dato anche il tasso di fallimenti e di resistenza associato a questo farmaco. Un’altra conseguenza della sovrapposizione del gene codificante la trascrittasi inversa e del gene codificante l’HBsAg è rappresentata dal fatto che alcune mutazioni (quali la M204I e la A181T), possono determinare la produzione di una forma tronca dell’HBsAg che si accumula all’interno della cellula, inficiando la produzione di particelle virali (21). Ciò porta ad un abbassamento della viremia che può mascherare la presenza di ceppi farmacoresistenti nel caso in cui il test di resistenza non venga utilizzato. Ciò evidenzia l’importanza di utilizzare il test genotipico anche nei casi in cui il rebound della viremia è contenuto, dato che le conseguenze della resistenza sono rilevanti anche in termini di oncogenesi. Studi precedenti hanno, infatti, evidenziato come l’accumulo di forme tronche delle proteine di superficie possa attivare fenomeni di oncogenesi virale. Ciò pone nella pratica clinica un serio dubbio sull’utilità dei test di resistenza “a spot”, mirati alla sola evidenziazione delle mutazioni principali. Solo la sequenza del genoma virale permette di riconoscere tutte le mutazioni di resistenza, di analizzare l’HBsAg, e quindi di valutare a tutto tondo i rischi di evolutività virale in corso di trattamento farmacologico, tenendo conto dello sviluppo di resistenze, di cross-resistenza, del livello di fitness virale (valutando numero e tipo di mutazioni in rapporto alla viremia), della presenza di escape-mutants in HBsAg, ed infine della presenza o meno di fattori potenzialmente collegati all’oncogenesi virale. |