| |
|
|
| |
| Reversibilità del processo fibrogenetico |
|
|
| Attualmente è considerata un processo di riparazione tessutale attiva, che si instaura in risposta ad un danno epatico cronico. Alcuni dati clinici ne hanno dimostrato la potenziale reversibilità [6]. In particolare, la fibrosi epatica viene considerata l'espressione dinamica di due processi biologici contrapposti, ossia la sintesi e la degradazione dei costituenti della ECM in risposta ad una noxa patogena persistente, come nel caso dell'infezione cronica da virus B o C. |
|
| In particolare, ciò che si osserva è un accumulo incontrollato di ECM fibrillare dovuto al mancato antagonismo dell'azione fibrolitica rimodellante [7]. Durante il processo fibrogenetico, l'accumulo incontrollato di matrice fibrillare riflette una diminuita espressione delle metallo-proteinasi (MMP) nelle cellule stellate contrapposta ad un incremento della sintesi dei loro specifici inibitori (TIMP, Tissue Inhibitors of Metalloproteases) [1,8]. |
|
| Nel processo fibrogenetico la ECM è soggetta ad importanti alterazioni sia nella quantità sia nella composizione. Negli stadi avanzati di fibrosi il fegato contiene un quantitativo di ECM circa sei volte superiore rispetto al normale, costituito prevalentemente da collagene (I, III e IV), fibronectina, undulina, elastina, laminina, acido ialuronico e proteoglicani. L'alterazione della matrice si riflette in nuove diverse proprietà della stessa: in primo luogo, le cellule epatiche si circondano di un microambiente biochimico e di supporto totalmente diverso da quello della condizione fisiologica. Sono pregiudicate, inoltre, importanti funzioni regolative e di comunicazione cellulare proprie della ECM. |
|
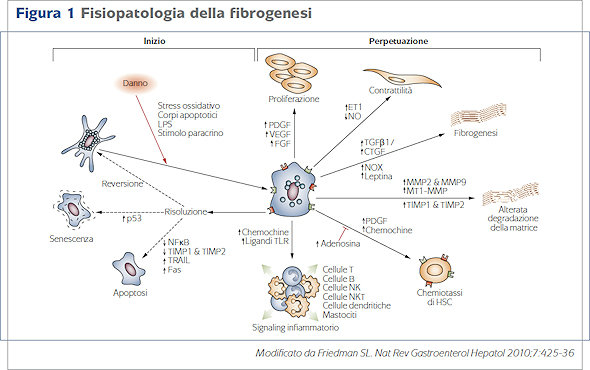
| Le cellule stellate epatiche (HSCs) sono le principali responsabili della produzione di ECM (figura 1). |
| |
 |
| |
| Nel fegato sano le HSCs sono localizzate al livello degli spazi di Disse e svolgono la funzione di depositi di vitamina A. Nel corso del danno epatico le HSCs si attivano e secernono citochine che perpetuano il loro stato di attivazione, esprimono molecole di adesione cellulare e modulano l'attivazione dei linfociti [9]. Le HSCs attivate, inoltre, si differenziano in miofibroblasti, migrano e si accumulano al livello del tessuto danneggiato, producendo matrice extracellulare e regolandone la degradazione [10]. |
|
|
|
|
|
|